-
スボレキサントとレンボレキサント
2020年08月23日
藤田医科大学の岸先生らが、スボレキサントとレンボレキサントについてのネットワークメタ解析の結果を報告され(文献1)、主観的尺度について興味深い報告をされていますが(詳細は省きます)、以前スボレキサントとレンボレキサントについて、高齢者ではどうかということを勉強会で文献的に検討したことがあり、岸先生らの論文の結果に触発されて、高齢者におけるデータを用いて解析したら何かでてくるのではないかと思い、手持ちのデータでネットワークメタ解析をしてみました(selection biasの問題があるので、よろしくないことではありますが)。
どのような点を明らかにしたかったかというと、文献1ではスボレキサントとレンボレキサントの18歳以上の原発性不眠症を対象とした介入試験の結果を解析対象としており、ポリグラフを用いた客観的指標については、例えば1か月時点での客観的持続睡眠潜時(LPS)は両群間有意差がでていない結果となっています(主観的指標では有意差あり)。しかし高齢者についての結果(SUNRISE1試験(文献2)および文献3)を見た感じでは、レンボレキサントは投与開始後1カ月時点での客観的持続睡眠潜時の短縮効果についても、プラセボと比較してなかなか良好なものがあるのではないかという印象をもっており、高齢者では有意な結果が出るのではないか、と期待したものです。
Rのnetmetaパッケージを用いて、頻度論によるネットワークメタ解析をrandom effectsモデルで解析してみました。評価尺度は投与1か月後のPSGによる客観的持続睡眠潜時(LPS)となります。結果は以下となりますが、有意差はなく、期待した結果は得られませんでした。しかしかなり良い線をいっている印象です。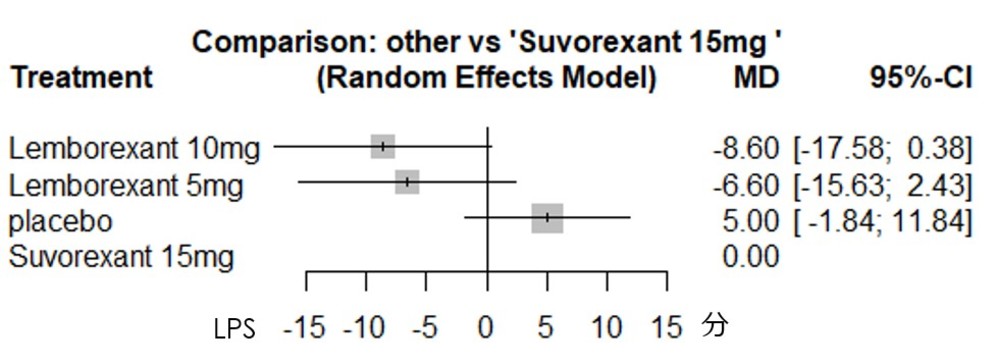
ネットワークメタ解析をきちんとするためにはデータの均質性や結果の一致性などを慎重に評価する必要があり、inconsistencyはありませんでしたが、均質性の評価はすっとばしています。もうちょっと症例数が蓄積すると結果が違ってくるかもしれません。オレキシン2受容体への選択性が高いことからノンレム睡眠を増加させることが期待されるとのことであり(文献1)、悪夢などの副作用がどうかについても気になるところです。
引用文献
1)Kishi T. et al. J Psychiatr Res. 2020 May 28;128:68-74. doi: 10.1016/j.jpsychires.2020.05.025. .
2)Rosenberg R, JAMA Netw Open. 2019 Dec 2;2(12):e1918254. doi: 10.1001/jamanetworkopen.2019.18254.
3)Herring W. et al. Am J Geriatr Psychiatry. 2017 Jul;25(7):791-802. doi: 10.1016/j.jagp.2017.03.004. Epub 2017 Mar 8. -
全般不安症とヨガ
2020年08月16日
全般不安症(GAD)に対するヨガとCBT、ストレス教育に関する介入試験がJAMA Psychiatry誌に掲載されていたので、現段階でのGADのエビデンスと一緒にまとめてみました。ヨガは2017年にはアメリカ人の14.3%が体験したそうです。大人気ですね。
全般不安症に対するヨガ、CBT、ストレス教育(文献1)
背景
・全般不安症は強い苦悩と機能障害を伴うが、およそ半分の患者しか治療を求めず、1/3の患者しか精神科専門治療を受けていないといわれている。
・認知行動療法(CBT)は全般不安症に対する心理療法の第1選択となっているが、コストや偏見などの理由により多くの患者がCBTを受けていない。薬物療法にも抵抗を感じたり、有効性が乏しい場合もあり、患者はヨガなどの代替療法を求めることがある・ヨガは人気があるが、不安に対する効果はよくわかっていない。
・伝統的にはヨガは姿勢や運動、呼吸の制御とリラクゼーション、瞑想などの訓練を伴う
・ヨガの人気は上昇しており、2017年には全米の約14.3%が健康のためのヨガを体験したと報告されている
・マインドフルネスに基づくアプローチはGADに有効性が確認されているが、ヨガの有効性はよくわかっていない。これまでの不安に対するヨガの効果についてのメタ解析の結果は結論がはっきりせず、より質の高い研究が求められている
・そこで今回ヨガのCBTに対する非劣性、ストレス教育に対するヨガおよびCBTの優位性、治療開始後6か月時点でのヨガのCBTに対する非劣性やストレス教育に対するヨガおよびCBTの優位性などを検証すべく、介入試験を行った
対象と方法
・Single blind無作為割付比較試験・試験期間:12週間
・18歳以上の全般不安症患者(DSM-V)。PSTD、物質使用障害、摂食障害の合併は除外。希死念慮を有する場合も除外。過去5年間に5回以上のヨガないしCBTセッションを受けたことがないこと。2週間以内に向精神薬投与を受けていないこと
・治療は3-6名の小集団毎に施行されブロックランダマイゼーションで治療法が決定された
・ヨガ群 N=93
・CBT群 N=90
・ストレス教育群 N=43・全ての群について、治療は1回120分、合計12回のセッションが3-6人の集団に対して行われ、各回20分の宿題が与えられた
・ヨガ群ではKundalini yogaがGuru Ram Das Center for Medicine and Humanologyにおいて開発された手法により行われた
・CBTは5つの治療コアモデュール(心理教育、認知再構成、漸進的筋弛緩法、不安への曝露、in vivo曝露訓練)を含み、メタ認知(不安への不安)をターゲットとしたが、マインドフルネスの要素は含まない
・ストレス教育はストレスの生理的、心理的反応や、カフェインやアルコール、喫煙などのライフスタイルの影響、レジリエンスに関与する要因、運動や食事の重要性などの教育が行われた
・主要評価項目は12週後のCGI-Iによる治療反応性(much improved ないしvery much improved)
・副次的評価項目は6か月時点での反応率
結果
・完遂率はヨガ群 64.5%、CBT群 74.4%、ストレス教育群 65.1%で有意差なし
・主要評価尺度の反応率については、ヨガ群(54.2%)はストレス教育群(33.0%)より有意に反応率が良好であった(OR 2.46 CI 1.12-5.42)
・CBT群(70.8%)はストレス教育群(33.0%)より反応率が有意に良好であった(OR 5.00 CI 2.12-11.82)
・非劣勢マージンΔを17.85%(反応率の差)に設定したところ、ヨガ群とCBT群の反応率の差は16.6%であり、ヨガ群のCIはマージンを超えるため、ヨガ群のCBT群に対する非劣性は支持されなかった。ただしCBTはヨガよりも有意に反応率が良好ということも統計的には示すことができなかった
・副次的評価尺度の6か月後の反応率は、CBT(76.7%)はストレス教育群(48.0%)より有意に良好であった
・ヨガ群(63.2%)はストレス教育群との有意差を示すことができなかった。
・またヨガ群のCBTに対する非劣性も支持されなかった
・ただし注意点としては、ベースラインにおけるうつ病の合併率(CBT群 24.4%対 ヨガ群 12.9%)が有意差があり、さらにフォローアップ期間での投薬率(CBT群 24.4% 対 ヨガ群 3.2%)が有意に異なったことがあげられる。そのためこれら交絡因子について調整したが結果は不変であった
結論
・ヨガはGADについて、ストレス教育より治療的効果が高そうだが、CBTに対する非劣性は支持されなかった
続いてGADに対するこれまでのエビデンスを概観してみます。
まず注目すべきは2019年のLancet誌(文献2)のネットワークメタ解析になりますGADに対する薬物療法のネットワーク・メタ解析(文献2)
背景
・GADの生涯罹患率は5.7%と言われており、12か月罹患率は65歳未満で約1.7%、65歳以上で3.4%と報告されている・GADは診断されにくい疾患であり、イギリスでの調査では一般人口の約3%がGADと診断可能であったが、そのうち約8%しか診断され治療を受けていなかったと報告されている。またプライマリケアにおいてGADが正確に診断されている割合は罹患者の34%であったとされている
・またGAD患者の62%が少なくとも1回以上の大うつ病エピソードを生涯に併発しているといわれている
・これまでの報告ではSSRIおよびSNRIの治療反応率が最も高く、60-75%と報告されている。Berezaら(2012)のレビューでは、第1選択薬での反応率は67.7%であり、第2選択薬での治療での反応率は54.5%と報告されている
・イギリスでの29131名の患者(大うつ病併発は除外)を対象とした報告では、平均3.7か月の治療後に46.0%の患者が処方されたSSRIや三環系抗うつ薬などを中断していたと報告されている(中断理由は不明)
・今回様々な薬物療法の有効性と安全性を比較するため、ネットワークメタ解析を行った
対象と方法
・1998年1月から2016年4月までに報告された89の介入試験(プラセボないし実薬対照) N=25441。71%がプラセボ対照
82%でDSMを診断に使用(罹病期間6か月以上が必要)・フォローアップ期間は4-26週間(中央値 8週間)
・全ての試験でHAM-Aを評価尺度として使用
結果
・クエチアピンの効果が最大(プラセボとのHAM-Aの差が―3.60点 CI -4.83 -2.39)だが、忍容性はあまりよくない
・デュロキセチン(MD -3.13 CI -4.13 2.13)、プレガバリン(MD -2.79 CI -3.69 -1.91)、ベンラファキシン(MD -2.69 CI -3.50 -1.89)、エスシタロプラム(MD -2.45 CI -3.27 -1.63)はいずれもプラセボより有意に治療反応率が良好
・その他ocinaplonは良好だがNが少なく根拠に乏しい
・パロキセチンとベンゾジアゼピンはサンプル数が多く、有効性もプラセボより有意に良好だが、脱落もまた多い
・ボルチオキセチンはプラセボと有意差なし(意外なことに)。忍容性は良好だが
結論
・安全性、忍容性を相互すると、プレガバリン、デュロキセチン、エスシタロプラム、セルトラリン、ベンラファキシンあたりが優れていそう
・ヒドロキシジン(アタラックス)が意外にも有効性、忍容性良好。しかし長期的には耐性などの問題もありそう
・ボルチオキセチンが結果が出せていないのが意外なところ(抗うつ薬としてはおそらくは優れているとの報告があるため)
ボルチオキセチンについては昨年、用量毎にGADに対する有効性などを検証したメタ解析が報告されているのでみてみます(文献3)
ボルチオキセチンのGADに対する有効性、安全性メタ解析(文献3)
背景
・ボルチオキセチンは直接的な受容体への作用(セロトニン3 、セロトニン7 、セロトニン1D 阻害作用、セロトニン1B 部分アゴニスト作用、セロトニン1Aアゴニスト作用)とセロトニントランスポーター阻害作用を併せ持つ複合的な作用を有する薬剤である。そのため大うつ病のみならず不安障害にも有効性が期待される・またSSRIと比較して海馬のBDNF発現量を有意に増加させるとの報告もある
・しかし近年のメタ解析ではボルチオキセチンのGADに対する有効性に関して否定的な結果を報告している(Fu et al 2016)。しかし機能障害やQOLについての評価はなされていない。そこで今回は有効性のみならず、その他の指標についてもメタ解析で評価してみた
対象と方法
・18歳以上のGAD(DSM)を対象としたプラセボ対照無作為割付試験
・有効性、QOL、機能障害を評価したもの
・反応はHAM-A50%以上の改善で定義
・寛解はHAM-Aが7点以下で定義
・QOLはSF-36(Short-Form 36 Health Survey)を尺度として用いた。機能障害についてはSDS(Sheehan Disability Scale)を用いた
・2012年から2014年に出版された4つの介入試験(ボルチオキセチン群 N=1074 、プラセボ群 613)、用量は2.5mg(N=308)、5mg(N=458)、10mg(N=308)
・試験期間はいずれも8週間
結果
・反応率はいずれの用量でもプラセボと有意差なし
・QOLはいずれの用量でもプラセボと有意差なし
・機能障害も同様
結論
・現段階ではボルチオキセチンは2.5mgから10mgまでの用量においてGADに対する有効性は確認できず(用量をいっしょくたにした過去のメタ解析では有効性を報告したものもあるが、用量毎にわけた今回の解析の方が臨床的には意義がある)
・安全性は良好であった
・まだNが少ないので、エビデンスの質としては低い
ボルチオキセチンについて一言
最後にボルチオキセチンについてフォローをしておきます。
私個人がボルチオキセチンを評価するのは、その安全性のみならず、2018年のLancet誌に掲載された21の抗うつ薬のネットワークメタ解析の報告(文献4)の図5の結果です。この図5の結果が2009年のMANGA studyと同じ解析(プラセボ対照試験を除外し、head-to-head試験のみで解析したもの)となります。
著作権の関係から図5は引用しませんが、論文そのものは無料で閲覧できますので、ご確認ください。ボルチオキセチンの有効性、安全性についての立ち位置がなんとなくわかると思います。また2016年のJournal of Affective Disorders誌の論文(文献5)においても、LHH(likelihood to be helped or harmed)=NNH/NNTという指標で解析した結果、ボルチオキセチンがデュロキセチン、エスシタロプラム、ベンラファキシン、セルトラリンなどの薬剤と比較して最も良好な数字を残しており、さらに5mgの試験を除外し10-20mgの試験のみで解析すると、ボルチオキセチンのNNT=5.3、NNH=63.3、LHH=11.9と群を抜いてよい数字となることがわかります。
ですので、大うつ病についてのボルチオキセチンのこれまでのエビデンスは比較的良好といえます。引用文献
1)Naomi M. et al. JAMA Psychiatry. Published online August 12, 2020. doi:10.1001/jamapsychiatry.2020.2549
2)April Slee et al. Lancet. 2019 Feb 23;393(10173):768-777. doi: 10.1016/S0140-6736(18)31793-8.
3)Bin Qin et al. BMJ Open. 2019 Nov 28;9(11):e033161. doi: 10.1136/bmjopen-2019-033161.
4)Cipriani A et al. Lancet. 2018 Apr 7;391(10128):1357-1366. doi: 10.1016/S0140-6736(17)32802-7. Epub 2018 Feb 21.
5)Citrome L. J Affect Disord. 2016 May 15;196:225-33. doi: 10.1016/j.jad.2016.02.042. -
アメリカ精神医学会のガイドライン草稿に思うこと
2020年08月09日
・10年ぶりくらいにアメリカ精神医学会の統合失調症のガイドラインが改訂されそうということで、その草稿(2019年12月版:文献1)が公表されていたのでざっと眺めてみました。
・草稿なので、最終版は改訂がされている可能性がありますが、薬物療法のところだけを眺めた感想を一言で述べるならば、BAP(文献2)の方が充実してていいんじゃないのか?ということでした。
・その理由としては、BAP版はちゃんとARMS、初発精神病エピソード、再発、維持療法と分けてそれぞれのエビデンスがかなり細かく網羅されているのに対して、APA版は急性期と維持療法期のみの記載となっていること。BAP版は陰性症状に対する項目や、過感受性精神病についての記述があることなどが挙げられます。以下BAP2019とAPA2019草稿版の一部をみていきたいと思います。
AMERICAN PSYCHIATRIC ASSOCIATION(APA)ガイドライン(2019年草稿)
Antipsychotic Medicationsの項目の概略
・クロザピンを除いては、特定の薬剤が別の薬剤に優れるとの十分なエビデンスはない
・初発エピソードについて第2世代抗精神病薬では薬剤間の有効性の差はあきらかではない。患者の特性と作用機序、副作用プロフィールに応じて選択する
・アドヒアランス不良の患者についてはLAI導入を考慮する
・副作用が問題なければ至適用量にて2-4週間は臨床症状の経過をみる(至適用量で2週間様子を見た時の反応率が20%未満であれば、その後の治療反応性が不良であるとの報告がある:Samaraら 2015)
・至適用量で2-4週間、2剤の抗精神病薬で治療反応性が不十分であればクロザピンを考慮する
・若年者では代謝系副作用や体重増加に注意
・抗精神病薬増強による増強療法も選択肢となる。ただし増強療法にこだわるあまり、クロザピン導入が遅れることは避けなければならない
・クロザピン使用に同意がない場合や忍容性不良の場合には、抗精神病薬高用量投与による利益はないことを示唆する限られたエビデンスがあり、副作用が増えるだろう。
・陰性症状ないしうつ症状があれば、抗うつ薬増強はメタ解析(Helfer ら 2016:文献3)により軽度の利益(うつ症状、QOLなどの改善に)があることが示されている。
・緊張病症状があればロラゼパムなどのベンゾジアゼピン投与は選択肢
・抗精神病薬の2剤併用については、コホート研究で単剤療法と比べて入院率や救急受診率が低かったとの報告(Tiihonenら 2019)があり、併用療法が単剤療法よりも有害であるとの明確な根拠もない。ただし副作用のモニタリングは重要である
・抗精神病薬治療に反応した場合には、その治療を継続することが推奨される(具体的な継続期間についての言及なし。短期間の精神病エピソード、物質誘発性精神病や気分関連精神病などについては抗精神病薬継続が必要ない場合もあるかもしれないとの記載はある。それ以外の場合には忍容性などに問題がなければ、ずっと続けるというようにも読み取れる)
British Association for Psychopharmacology(BAP)ガイドライン2019年版
ARMSについて
・ARMS(At Risk Mental State)患者は12か月以内での精神病性障害移行率は15-30%で、3年で36%以上といわれている(Fusar-Poliら 2012)
・減弱精神病症状(APS:attenuated psychotic symptoms)への介入について:オフラベル投与にはなるが、超低用量抗精神病薬投与(初発精神病よりも低用量)は考慮しうる(推奨度D:BAPガイドラインの推奨度は文献2を参照してください)。しかし投薬を好まず心理療法的介入を好む場合も多い
・予備的なエビデンスだが、低用量抗精神病薬、CBT、支持的精神療法いずれもAPSを改善しうるとの報告がある。ただし抗精神病薬とCBTの併用はCBT単独と比較してより有益であるとのエビデンスはない(Yungら 2011)。
・6 studiesのメタ解析ではCBTは支持的なneeds-based interventionと比較して有意にAPSを改善したと報告している(Davis 2018b)。また家族療法もAPSに有効であったと報告されている
・ジプラシドンはプラセボよりも6か月予後が有意に良好であったとの介入試験の報告がある
精神病顕在発症を防ぐための介入
・低用量抗精神病薬ないしCBTが精神病顕在発症を防ぎうるかについて検討したメタ解析では抗精神病薬のNNT=7、CBTのNNT=13と報告されている(van der Gaagら 2013)
・ジプラシドン対プラセボの精神病顕在発症進展リスクについての介入試験では有意差が検出できなかった。規模が小さかったことも原因
・CBT、アリピプラゾール+ケースマネジメント、プラセボ+ケースマネジメントの3群比較試験では群間の有意差はなかった。有意差はなかったがCBTが良好な傾向があった(52週の精神病移行率:CBT:19%、アリピプラゾール:26.8%、プラセボ:30%)。CBTは脱落率も低かった(Bechdolfら 2016)
・抗精神病薬を用いた介入試験では、抗精神病薬の脱落率が高く、ARMS群における忍容性が不良であることを示唆している
個別CBTは薬物療法の代替として考慮しうる(推奨度D)・オメガ3不飽和脂肪酸については、1つの介入試験で有意な精神病発症予防効果が報告されたが、その後2つの大規模試験では否定的な結果となった
初発精神病
・一過性精神病なのか、統合失調症なのか、気分障害に伴う精神病なのかで予後が異なる
・抗精神病薬を使用せず、精神病に対するCBTを行う選択肢がある。投薬を拒否した群に対してCBTpを6か月施行した介入試験では症状改善に有用であったとの報告がある(Morrisonら 2014)。
・CBTpと抗精神病薬、両者併用を比較した小規模試験では、1年以上後の症状改善度においてCBTp群と抗精神病薬群とで有意差なく、併用群でCBTp単独よりも有意に良好な結果であった。(Morrisonら 2018)。
・小規模の試験結果しかないため、CBTpが抗精神病薬と同等の有効性を有するとのエビデンスは非常に限定的であり、自傷リスクが少なく、投薬が困難なケースについては心理療法単独を考慮してもよいかもしれない
・統合失調症では低~中用量抗精神病薬単剤療法が第1選択
・ハロペリドールについては2mgで大半がD2/3受容体占有率が60%を超えると報告されており、D2/3受容体占有率が80%を超えるとプロラクチン上昇やEPSなどのリスクが増加する
・ハロペリドールについてはパーキンソンズム出現の中央値は初発精神病では2mg、非初発であれば4mgといわれている
・オランザピンの初発精神病の有効平均用量は7.7mgと報告されている
・EUFEST studyなどのオープン試験での報告では、初発精神病の抗精神病薬有効用量として、リスペリドン2-4mg、ハロペリドール2-5mg、クエチアピン400-500mg、アミルスプリド 450mg、オランザピン 10mgを推奨している
・薬剤選択については、特定の薬剤が別の薬剤と比較して有意に優れているとの明らかなエビデンスはない
・リスペリドン、オランザピン、アミルスプリドがハロペリドールより良好であったとのネットワークメタ解析の報告があるが、studyの質は低~中等度である(Lancet Psychiatry. 2017 Sep;4(9):694-705.)
・治療開始6か月時点で寛解基準を満たすのは観察研究では中央値40%(17-78%)と2012年に報告され、その後の報告では59%(Gaebel 2014)、60%(Chiliza 2016)との数値が報告されている。一方で経過中の一時点でも症状寛解を達成する割合は55-70%と報告されており、Gaebel (2014)は91%と報告している
・OPTIMISE試験(Kahnら 2018)では、初発統合失調症446名を対象に第1相で4週間アミスルプリド投与され、非寛解群が第2相で6週間アミスルプリド継続ないしオランザピンに無作為割付され、非寛解群が第3相でクロザピンにスイッチされた。446名中33%は脱落し、64%は寛解し、3%が全ての相終了後も非寛解だった。4週間のアミスルプリドで56%が寛解。その後第2相でアミスルプリドに割付された47名のうち6週間で45%が寛解。全体として10週間でアミスルプリドで82%が寛解。ただし脱落者が非寛解と仮定すると、寛解率は60%に低下する
・初期治療は6週間行い、十分な反応がなければ、次の薬剤に変更を考慮する
・初発精神病後に抗精神病薬継続は再発リスクを半分に低下させる。Leuchtら(2012)は65試験のメタ解析を行い、1年間の再発率は抗精神病薬を中止すると64%、継続すると27%であったと報告している。Zipurskyらは2014年にメタ解析により副作用の問題がなければ投薬は中断すべきではないと結論付けている
・観察研究によれば、一部の患者においては抗精神病薬を中止可能であることが報告されている。初発の非気分障害精神病のデンマークでのコホート研究では、1-5年のフォローアップで25%が寛解しかつ抗精神病薬投与を受けていなかった。10年後はその数が30%に増加した。5年時点で投薬を受けておらず寛解していた患者は10年時点でそのうち87%が無投薬での寛解を維持できていたという
・Huiら(2018)の10年予後の結果を引用し、少なくとも3年間投薬を維持することはその後の長期予後を良好にする可能性について言及されている
・BAPガイドラインは少なくとも2年間の継続を推奨
・LAIについてはアドヒアランス不良患者に適していると思われ、早期からの導入により再発を防ぐとの報告は信頼に値するが、研究デザインと対象群の非均一性の問題により、治療における位置づけを確信を持って評価することはできない
(BAPガイドラインには含まれていないが、初発精神病に関して含まれていてもよさそうなその他の報告)
・初発精神病の治療反応率については、522名がリスペリドンとハロペリドールに無作為割付され治療反応性(PANSSで20%以上の改善度で定義)が観察された試験(Am J Psychiatry. 2006 Apr;163(4):743-5.)があり、治療期間の中央値206日間で全体の反応率は400名(77%)。反応した400名の中で1週目で反応したのは23.3%、2週目23.3%、3週目18.5%、4週目12.5%(4週目までで全体の8割)。8週目11.2%、さらにそれ以降で反応したのは11.3%。反応を達成した時の用量は1mgが15.5%、2mgが29.8%、3mgが27.3%、4mgが16.8%、4mg以上が10.8%。そこまで高用量使用しなくても反応は得られる
・中国からの報告であるが(例えばLancet. 2019 Sep 14;394(10202):939-951のような有名なメタ解析では中国大陸からの報告というだけで質に問題ありとのことで解析対象から除外されたりしている)、未治療の初発統合失調症200名に対してリスペリドン、オランザピン、アリピプラゾール、クエチアピン、ジプラシドンが比較され、リスペリドンがオランザピン、アリピプラゾールより有意にBPRS改善度が良好だったとの報告がある(Ann Gen Psychiatry. 2017 Dec 22;16:47)
・198名の初発精神病患者についてアリピプラゾール5-30mgとリスペリドン1-6mgが比較され、陽性症状の反応率は有意差なく(ARI対RIS:62.8% 対56.8)、陰性症状はアリピプラゾールが良好だったがアカシジアが多く、アカシジアの観点からはリスペリドン少量が、代謝系副作用の観点からはアリピプラゾールが推奨されるとの結論であった(Schizophr Bull. 2015 Nov;41(6):1227-36. )
・TEA試験(Lancet Psychiatry. 2017 Aug;4(8):605-618)の結果は重要と思われる。
12-17歳の若年初発精神病患者113名に対してクエチアピンER(ターゲット用量600mg)ないしアリピプラゾール(ターゲット用量20mg)の無作為割付比較試験が行われ、12週間で両薬剤に有効性に有意差はなく、クエチアピン群とアリピプラゾール群の体重増加量の差は3.33kg、2週目のアカシジア出現率がアリピプラゾール群60%、クエチアピン群30%で有意差あり(その後有意差なし)。振戦がアリピプラゾール群91%、クエチアピン群79%。鎮静がアリピプラゾール群97.1%、クエチアピン群89.2%(有意差あり:これは意外な結果)・若年者の初発精神病に対する薬物療法は、副作用出現率が極めて高く注意を要する
急性精神病エピソード(再発)
・再発に伴い抗精神病薬に対する反応性が悪化することが報告されている。メタ解析(Leucht 2017)ではPANSS/BPRS得点が少なくとも20%以上改善する反応率については、反応率は50%と報告されている(プラセボでは30%)。さらに50%以上改善する割合は23%でプラセボでは13%と報告されている
・抗精神病薬の有効性に関しては同等であり、治療抵抗性についてはクロザピンが最善となる
・用量は初発エピソードよりも一般的に多くなる。PETを用いたstudyでは、D2受容体占有率が60%を超せば治療反応性が増大し、線条体ないし下垂体D2受容体占有率が80%を超すとEPS、高プロラクチン血症のリスクが高まると言われている。アリピプラゾールは例外であり治療用量である10-15mgでD2受容体占有率は85%以上と言われている。
・治療開始後2週間でPANSS改善度が20%未満の非反応群は、治療開始後3か月時点でも84%が非反応群であったと報告されている(Kinon 2008)
・罹病期間が長引くにつれて、治療反応性が悪化することは介入試験の結果から統計的に有意であることが示されている(Leucht 2012)
・このことは部分的にはドパミンD2/D3過感受性精神病で説明がつくかもしれない。Howesらは一部の患者でD2/D3受容体の発現亢進が起きていることを報告した
・D2受容体遮断長期治療の結果、過感受性精神病による病状悪化が起こりうるなら、D2受容体部分アゴニストのアリピプラゾールでは長期治療後の再燃が起こりにくいことが推測されるが、現在までのところそのことを明確に支持するデータはない
・また、D2受容体の過感受性が形成されると、維持中の抗精神病薬を中断した際の反跳性精神病も起こりやすくなることが推測される
・抗精神病薬中断による精神病症状の増悪は疾患の自然経過と反跳性精神病の区別が難しいため、臨床的に反跳性精神病を見分けることは困難である。またコリン離脱性反跳症状との区別も困難である
・ただし、この問題は抗精神病薬を中断した場合と持続した場合の介入試験の結果の事後解析から推測が可能であり、Emslryら(2018)は、中断後の症状増悪の両群間の特徴の類似性(治療反応性も含め)から、再燃は自然経過によるものが大半と結論付けている(コメント:ただしこの試験はパリペリドンLAIによるものであり離脱症状を正しく評価できたとはいえないのではないか)。
・さらにTakeuchiら(2017)は、中断後の症状増悪は急速な増悪ではなく、徐々に増悪がみられることから、反跳性精神病にあたらないのではないかと考察している。
・メタ解析(Leucht 2012)でも、急な中断群と漸減群とで再燃リスクが変わらないことが示されている
以上の結果は、ドパミン過感受性が症状再燃の誘因であるとの仮説が一貫して支持されるものではないことを示唆しているうつ症状に対する抗うつ薬増強について
・Helferら(2016:文献3)は統合失調症患者について、抗うつ薬増強の安全性と有効性についてのメタ解析を報告した。全体としてうつ症状の改善についての効果量-0.25(CI -0.38 -0.12)でありプラセボよりも有意に良好であり、うつ症状の重症度が増せばより効果量が高まるとの結果であった。
・Gregoryら(2017)は統合失調症にうつ病を合併した症例(陰性症状とうつ症状との鑑別により有用とされるCDSSを用い、うつ病の診断がきちんと下されたケースについての報告)についての薬物療法のメタ解析を行い、抗うつ薬(多くがSSRI)はNNTが約5で有効であると報告している。ただし含まれた26の試験の質は中から低品質であり、26のうち19の試験で現在のRCTの報告基準を満たさなかったとされている。
・抗うつ薬を使用するかどうかについては、臨床医は患者とこれまでの介入試験の結果などについて話し合うこと。もし抗うつ薬の効果が認められないならば中止すべきである。
(コメント:BAPガイドラインでは陰性症状についての項目で文献4のGallingらの報告が取り上げられており、うつ症状についての項目ではなぜかGallingらの報告についての記載がありません。しかし個人的には統合失調症における抗うつ薬増強の現段階で最も質の高いエビデンスの1つがGallingらの報告ではないかと思われるため、この報告が入っていないのは釈然としません。ちなみにGallingらの報告は、最初から抗うつ薬の増強を行った試験などは除外しており、より抗うつ薬増強の有効性の評価に特化した試験のみを抽出しており、Helferらの報告よりも質が高いことが期待されるものです。Gallingらの報告では、統合失調症に併発するうつ症状に対して抗うつ薬増強はプラセボに対して有意差がないとするものでした。この結果を信じるならば、日本神経精神薬理学会の現在のガイドラインの記載が最も妥当ということになります。ただしうつ症状が重度の場合には個別に慎重に判断すべきとは思われます)
最後に
・APAガイドライン草稿の統合失調症における抗うつ薬の増強については2016年のHelferらの報告(文献3)が引用され、Gallingの2018年の報告(文献4)は引用されていません(BAPでは陰性症状の項目で引用されている)。結論もHelferらの報告に準じたものであり、違和感を感じます。
・BAPガイドラインは引用されている文献も豊富で、全体的にこれまでのエビデンスの復習としてもとても有用と感じました。
文献1)https://www.psychiatry.org/psychiatrists/practice/clinical-practice-guidelines
文献2)J Psychopharmacol. 2020 Jan;34(1):3-78. doi: 10.1177/0269881119889296. Epub 2019 Dec 12.
文献3)Helfer B, et al. Am J Psychiatry. 2016 Sep 1;173(9):876-86. doi: 10.1176/appi.ajp.2016.15081035. Epub 2016 Jun 10.
文献4)Galling B, et al., Acta Psychiatr Scand. 2018 Mar;137(3):187-205. doi: 10.1111/acps.12854. -
思春期初発精神病に対する抗精神病薬と心理療法
2020年07月29日
・Lancet Psychiatryに思春期初発精神病に対して抗精神病薬(主にアリピプラゾールなど)と心理療法(CBTと家族介入)の単独ないし併用の小規模介入試験(主要評価項目は将来の大規模試験のfeasibility(実現可能性))についての報告(文献1)がありました。
・ここで用いられたCBT(詳細は文献4など)はNICEガイドラインにおいて標準的に推奨されている手法であり、精神病症状に限らず、自信を回復するなど、幅広く治療ゴールを設定するものとなります。
・ちなみに精神病症状を直接のターゲットとしたCBTの臨床試験(幻聴をターゲットにしたCBTの最初の大規模な質の高い臨床試験であるCOMMAND試験:文献2)の結果は重要であり、さらに標準的なCBTのような大変な手間とコストのかかる手法ではなく、PCとバーチャルリアリティーを活用したより簡易なAVATAR療法とよばれる、大変面白い手法についての報告(文献3)もおさえておくべきかと思います。
背景
・早期発症精神病は18歳未満に発症する初発精神病をさす。イギリスでは発症率は10万人あたり5.9人と報告されている
・早期発症であることは予後不良と関連する可能性もあり、病前機能が悪かったり、DUPが長かったり、初発症状が重篤であるとさらに予後の悪化要因となりうる。
・2015年のシステマティックレビューでは若年精神病患者への治療は抗精神病薬が主流であることが示されている。しかしながらその有効性に関するエビデンスは成人に比較して乏しい。これまでのメタ解析では、抗精神病薬は小さいながらも有意な治療効果(PANSS、社会機能、全般的機能に対して)を有することが報告されている。しかし少数の質の低いstudyからなる報告であり、プラセボ群でも改善度が大きく、代謝系副作用も大きかったことなども懸念されるものである
・精神病に対しての心理療法については、システマティックレビューでは、18歳未満を対象としたCBTないし家族介入についての報告はこれまで存在しないとされている。25歳未満を対象としたCBTと家族介入については、8つの低品質の報告があり、両者の組み合わせで小さいながらも有意な効果があるとされている
・2015年以降では、小規模(n=30)の18歳未満精神病患者を対象とした非無作為化試験(CBT対家族介入対通常治療)が行われており、思春期精神病に対しての心理療法の有効性を比較する臨床試験が実現可能であることが示された
・NICEガイドラインは早期発症精神病に対して心理療法を推奨しているが、その根拠は成人についてのエビデンスを外挿したものであり、若年精神病へのエビデンスは乏しい。そこで今回思春期初発精神病患者に対しての心理療法を抗精神病薬と比較する臨床試験の実現可能性について検討した
方法と対象
・無作為割付single bilnd比較試験
・14-18歳の初発精神病患者(メンタルヘルスサービス受診1年以内)
・PANSSの妄想ないし幻覚の下位尺度が4点以上で1週間以上持続
・ICD-10で統合失調症ないし統合失調感情障害ないし妄想性障害ないしEIP(Early Intervention in Psychosis)の初発精神病のエントリー基準に合致
・過去3か月以内に構造化された心理療法ないし抗精神病薬を受けたものは除外
・抗精神病薬投与群 N=22
・CBT+家族介入群 N=18
・抗精神病薬+心理療法併用群 N=21
・CBTは合計26時間(おおよそ週に1回)+4回のブースターセッション
・家族介入は月に1回程度(その他CBT後に同意者については家族と情報共有)
・CBT開始後に患者と治療者は問題点を同定し、CBTの治療ゴール(自信を回復するなど精神病症状と関連しないものもゴールに設定しうる)を共有し、ゴールを達成するための個別化されたプランが開発された
・ついで、認知再構成のための手法(幻聴などに耳を傾けることの利益や不利益を検討する、適応的な対処法や睡眠衛生に関する教育、ロールプレイなども含む)などが展開された
・最後に再発予防のための地固め段階が実施された
・家族介入はbehavioural family therapy approachに基づく介入が実施された
・薬物療法については、NICEガイドラインに準拠した処方が行われた。介入直後に開始され、少なくとも3か月間、できれば6か月以上継続することが推奨された。処方内容と用量は各主治医に任された
・主要評価項目は治療の実現可能性であり、試験への参加率とCBTへの参加率、薬物療法へのアドヒアランス、治療への忍容性
・副次的評価項目は、ベースライン、3か月後、6か月後、12か月後のPANSS total(25%の改善を minimal improvement、50%の改善をgood clinical response、などと定義。さらに社会的機能、主観的回復、不安及びうつ(HAD)、物質使用障害などを評価
結果
・試験への参加率は68%、6か月時点での試験への非脱落率は全体で84%
・心理療法群(単独ないし薬物療法併用)においては82%が6回以上のCBTを受けた。抗精神病薬群(単独ないし心理療法併用)においては65%が6週間以上の薬剤投与を受けた。心理療法へのアドヒアランスは概ね良好で、薬物療法については中等度のアドヒアランスであった。
・抗精神病薬で使用された薬剤はアリピプラゾール(約50%)、リスペリドン(約25%)、クエチアピン(約25%)が最も多かった
・抗精神病薬単独群は6か月後にPANSS totalで6.2点改善、心理療法単独群は6か月後に13.1点改善、併用群は13.9点改善。PANSS totalで50%以上改善した割合は、抗精神病薬単独群は6か月後で22%、心理療法単独群では31%、併用群では29%
・重大な有害事象は抗精神病単独群の13%(2名が重大な暴力)、心理療法群では24%(自殺企図1名、2名が重大な暴力、2名が内科入院)、併用群では35%(精神科入院3名、自殺企図1名、重大な暴力1名、内科入院1名)など
・3か月後の時点で、9名がPANSS totalで12.5%以上の悪化を示した。4名が心理療法単独群、3名が抗精神病薬単独群、1名が併用群、1名は治療拒否群であった
結論
・若年初発精神病患者に対して、心理療法と抗精神病薬の比較を行う大規模介入試験は可能である。しかしいくつかのサイトでの患者エントリーは順調にいかなかったことから、今後工夫が必要と思われる。また一部の患者は治療に参加せず今後さらに大規模な臨床試験を行うために試験デザインの改良が必要である
・今回施行した3群の安全性は概ね良好であり、抗精神病薬を使用しない心理療法が、使用群と比較して症状増悪を有意にもたらすとの証拠は得られなかった
全ての群でPANSS変化量は6か月で6-14点、12か月で12-20点であり、臨床的に有意な最小変化量として15点以上(治療者評価)といわれているため、いずれの治療法も臨床的に意義があると思われる・治療行為に起因した重大な有害事象はいずれの群でもみられなかったと思われる
・Nが少なく治療効果の判定はできないが、数値的には心理療法単独、心理療法+抗精神病薬併用が同程度の改善度であり、心理療法(CBT+家族介入)単独でもいけそうな印象がある(ただしかなりの手間がかかる)
・今後大規模試験での検証が必要
小規模試験のため結果の一般化はできませんが、若年者に対してはARMSのみならず、精神病顕在発症後も心理療法が有力な介入手法となりうる可能性があることを示唆する報告であり、今後の大規模試験の結果が注目されます。
1)Morrison AP, et al. Lancet Psychiatry. 2020 Jul 7:S2215-0366(20)30248-0. doi: 10.1016/S2215-0366(20)30248-0. Online ahead of print.
2)Birchwood M, et al. Lancet Psychiatry. 2014 Jun;1(1):23-33.
3)Craig TK, et al. Lancet Psychiatry. 2018 Jan;5(1):31-40.
4)Anthony P. Morrison Psychosis. Pages 271-281 Volume 9, 2017 - Issue 3 -
polygenic risk scoreについて
2020年07月23日
・AJP in advanceにpolygenic riskと単極性うつ病の予後についての報告(文献2)がでていましたので、polygenic risk score(PRS)などについて少しまとめておきます。
・感想としては、有用な場面もあるかもしれないけど、一塩基多型(SNP)の組み合わせで構成されるPRSは、精神疾患においてはそこまで強力な予後予測ツールには現段階ではなりそうもないかなというところです。ただし、この概念を知っておくことは必要かと思いました。
polygenic risk score(文献1より)
・それぞれの遺伝子変異(主に一塩基多型)は疾患リスクにはわずかな影響しか与えないが、そのような変異が多数重畳することで、疾患リスクの有意な増加をもたらしうるという知見がゲノムワイド関連解析により得られつつある。
・リスクに関連する一塩基多型の数により疾患リスクを評価する指標として多遺伝子リスクスコア(polygenic risk score:PRS)が提唱されている。
・PRSは多くの症例対象研究により実際に疾患リスクの増加と関連することが報告されている。同時にコホート研究でもその関連性が報告されている。PRSの潜在的な有用性を認める報告は多いが、臨床的な有用性はまだ確立されていない。PRSが果たして疾患の発症リスクや予後を予測しうるものなのか?そのような疑問に答えるため、研究は集団を対象とした症例対象研究から、個人を対象としたものにシフトしつつある。
・各個人の保有する疾患リスク対立遺伝子について、それぞれの効果量(binary dataであれば例えばlog(OR))で重みづけし、合計していく。この方法は最も単純なPRSの計算法であり、リスク遺伝子間や遺伝子と環境間の相互作用がないことを仮定している。実際には相関構造を仮定し、Bayesian LDpred approachなどがPRSの計算に用いられている。
・PRSを実用的なツールにするためには、これまでの対照群と比較した相対リスクから、疾患発症の絶対リスクに変換する必要がある。現存する疾患のリスク予測モデルには、心血管疾患および糖尿病の10年リスクを予測するものがあり、それらは臨床所見、臨床、生化学、生活習慣、および過去のリスク因子の組み合わせからなる。これらのモデルは良好な予測率(AUC(実際の疾患群の分布と予測群の分布の重なり)は80~85%)を達成し、予防と公衆衛生のための臨床ガイドラインに含まれている。・多遺伝子リスクスコアは、これらのリスク予測モデルにとって代わるほどの高いAUCは期待できず、これらのリスク予測モデルの代替ではなく、モデルを補強する補助的因子として考慮されることが妥当であろう。
・現在の重要課題は、疾患における遺伝的リスクの高い個人を同定することである。このことにより、個人がスクリーニングに参加したり、生活スタイルの修正を行ったり、予防的介入を受けるための動機づけとなりうる。ただし遺伝子だけですべてが決まるわけではないため、誤解をさける必要もある。・乳癌においては、303の遺伝子変異(SNPs)に基づくPRSによりAUCが0.63、PRS1単位増加あたりオッズ比 1.61との結果が報告されている。この結果を言い換えると、PRSが平均的スコアの女性と比較して、上位1%の女性はエストロゲン受容体陽性乳癌の発症リスクが4倍であり、下位1%のPRSの女性についてはエストロゲン受容体陽性乳癌の発症リスクが1/6となるということになる。PRSはスクリーニングにおいて活用可能となる。
・PRS上位の女性については、スクリーニング頻度を増やしたり、開始時期を早めるなどの対策が考えられる。イギリスではマンモグラフィーによるスクリーニングは47歳以上の女性に提供され、その後10年間での乳癌リスクは2.6%と報告されているが、PRSが上位20%内にある女性については、40歳未満で同等のリスクに達し、下位20%の女性は年齢によらず同等のリスクに到達することはないと報告されている。
精神疾患とPRS
【大うつ病】
・大うつ病の多遺伝子リスクスコアは、最近のゲノムワイド関連研究の結果を用いて計算することができる。Wrayらは、有意な44のSNPを同定し、PRSの上位10%の人は、下位10%の人に比べて大うつ病リスクが約2.5倍に増加していることを報告した。
・しかし、このスコアのAUCは0.57であり、大うつ病遺伝形質の分散の2%しか捉えておらず、残りの98%はPRSでは捉えられていない。したがって、個人のうつ病リスクは、測定可能な遺伝的リスクスコアの2%と、遺伝的ないし環境的要因による98%の未測定の成分から構成されている。
・遺伝的リスクが非常に高い個人であっても、PRSで説明可能なリスクは未測定成分に圧倒されてしまう。したがって、うつ病のPRSはまだ有用ではない。
【統合失調症】
・統合失調症では、現在のPRSスコアが統合失調症遺伝形質の分散の7%を占め、AUCは0.61と予測能力は大うつ病よりも高いが、臨床的に有用なレベルではない。
・統合失調症では遺伝率(heritability:全表現型分散と相加的遺伝分散の比。親から子へ遺伝する確率ではない。直感的には実現遺伝率の概念がわかりやすい)が65-80%と大うつ病の37%よりも高いが、多遺伝子スコアは一般的な予測には意味がない。
・ただし早期の診断やより正確な診断のためにPRSが有用な可能性がある。例えば、初発精神病では、統合失調症のPRSが他の精神病診断と区別できる可能性が示されている(PRSの上位20%の人は、その後統合失調症と診断されるリスクが約2倍に増加する)。これは低い予測能力であるが、初発精神病症例の中での予測であり、(1)一般集団のジェノタイピングを必要とせず、精神病患者のみを対象としていること、(2)主要な判断(治療/不治療など)には関係ないが、ケアプランに役立つ可能性のある追加情報を提供できること、などの理由から、有用かもしれない。
・本題にうつる前に、現在までの単極性うつ病患者が双極性障害に移行するリスクについての報告をまとめておきます。
・文献4のメタ解析とシステマティックレビューによれば、12-18年間のフォローアップ期間において単極性うつ病患者の双極性障害移行率は22.5%とされています。またメタ解析により3つのリスク因子が同定されています。
・それらは若年発症(g=-0.33)、精神病症状の合併(OR=4.76 CI 1.76-12.66)、双極性障害の家族歴(OR=2.89 CI 2.01-4.14)でした。
・次いで、文献3では、デンマークでの大規模前向きコホートにより、これらリスク因子について再現性があるのか検討されました。
・対象となったのは1995年1月1日以降2016年12月31日(の8週間前)までに大うつ病の診断を最初に受け退院した患者(レジストリとしてthe Danish Psychiatric Central Research Register (DPCRR)を使用)で91587名が対象となりました。
・リスク因子として、性別、出生地(都会か田舎か)、初発うつ病エピソードにおける治療環境(外来か入院か救急外来か)、うつ病エピソードが再発性か単回か、初発うつ病の重症度(軽度、中等度、重度、精神病症状を伴う)、初発時の年齢、初発うつ病エピソード以前の精神疾患の既往(物質使用障害、気分に一致しない精神病性障害、神経症、身体表現性障害、強迫性障害、摂食障害、パーソナリティ障害、精神遅滞、自閉症スペクトラム、ADHD)、両親の精神疾患の既往が設定されました。
・平均7.7年間の追跡の結果、経過観察中3910名が双極性障害に移行し、20年間での累積移行率は女性の方がやや移行率が高く(8.7%対7.7%)、双極性障害への移行のリスク因子としては、親の双極性障害罹患歴(調整後ハザード比 2.60 CI 2.20-3.07)であり。親が双極性障害である場合の20年間の累積移行率は25%でした。次いで初発うつ病エピソードでの精神病症状合併(調整後ハザード比 1.73 CI 1.48-2.02)、気分と合致しない精神病症状の合併ないし既往(調整後ハザード比 1.73 CI 1.51-1.99)、初発エピソードでの入院治療(調整後ハザード比 1.76 CI 1.63-1.91)などが有意なリスク因子として抽出されました。
・そのほかの有意であるが影響の小さな要因としては、都会よりも田舎での出生(統合失調症の発症リスクとは逆であることが興味深いところです)、反復性のうつ病エピソード、初発エピソードが重症であること、アルコール使用障害の既往、親の単極性うつ病の既往などでした。
・メタ解析で同定されたリスク因子のうち、家族歴、精神病症状の併発については有意なリスク因子として抽出されましたが、若年発症であることはその後の双極性障害移行リスクとして有意なものとしては抽出されませんでした。その理由としてレジストリに基づく研究では18歳未満、特に10-14歳の小児患者については双極性障害移行率を過小評価してしまう(よりフォローアップでの観察の細やかな臨床研究と比較して)傾向があるためではないかと考察されています。
単極性うつ病と診断された患者のpolygenic riskと双極性障害ないし精神病性障害進展リスク(文献2)
背景
・双極性障害患者や精神病性障害患者においては、しばしば双極性障害ないし精神病性障害診断前にうつ病エピソードを経験している・多くの場合、うつ病エピソード中にメンタルヘルスケアの専門家を受診する。この段階で将来の双極性障害ないし精神病性障害進展リスクを評価できれば患者の予後を改善するために有用と思われる
・しかしながらうつ病有病率は高く、一方で大半のうつ病患者は双極性障害ないし精神病性障害には進展しない
・双極性障害ないし統合失調症については、その発症について一部は遺伝的要因の影響が考えられている
・これまでにうつ病、双極性障害、統合失調症の発症リスク遺伝子に重複があることが報告されている。しかしながら一部のリスク遺伝子は疾患特異的である。そこでうつ病患者において、遺伝子的に将来双極性障害ないし精神病性障害に進展するリスクの高い一群を同定可能な可能性がある
・一方で両親の罹患歴は遺伝子的な発症脆弱性のマーカーとして用いられてきた。
・しかしながら両親の病歴があると、より早期に受診したり、治療者により診断されやすかったりするなどの傾向があることが推測されるため、家族歴以外の遺伝的マーカーが必要である。
・そこでpolygenic risk scores(PRSs)に着目し、大うつ病患者がその後双極性障害ないし精神病性障害に進展するリスクを予測する遺伝子的マーカーとなりうるかどうかを後ろ向きに検討した
方法と対象
・iPSYCH Danish case-cohort study(iPSYCH2012)からデータを抽出
・1981年から2005年の間にデンマークで生まれ、2012年12月31日までに公費の精神科病院で気分障害、統合失調症、自閉症、ADHD、摂食障害の診断を受けたすべての症例と、1981年から2005年の間に生まれ、1歳の誕生日まで生存し、母親が明らかなデンマーク人から抽出された3万人の無作為サンプルが対照となった。
・症例はDanish Psychiatric Central Research Register: DPCRR)から同定された。このレジストリには、1969年から1994年までのデンマークの精神科病院の入院患者におけるすべての精神科的診断と、1995年以降の入院患者、外来患者、救急部における診断が含まれている。
・DPCRRの診断は、1969年から1993年まではICD-8、1994年以降はICD-10に基づく。iPSYCH2012に含まれた症例は、2012年までのDPCRRからエントリーされている。
・遺伝子型判定については、全症例に対して出生時に採取された血液サンプルにより行われた
結果
・N=16949 、患者の80%が25歳未満で大うつ病と診断。女性が69%。61%が外来患者。中等度うつ病エピソードが44%
・フォローアップ期間の中央値は7.3年(最大21.1年)
・双極性障害のPRSと統合失調症のPRSは中等度の有意な相関あり(r=0.40)、大うつ病と双極性障害のPRSについても弱い有意な相関あり(r=0.14)、大うつ病と統合失調症のPRSについても弱い有意な相関あり(r=0.13)
・調整後は双極性障害のPRSsはその後の双極性障害進展リスクと有意な関連を示した(PRS得点が1SD分増加すると調整後ハザード比で1.11 CI 1.03-1.21ほどリスクが増加)。一方で統合失調症のPRSsは調整後はその後の双極性障害進展リスクと有意な関連は示さなかった
・統合失調症のPRSsのみが、その後の精神病性障害への進展について有意な関連を示した( PRS得点が1SD分増加すると調整後ハザード比で1.10 CI 1.04-1.16ほどリスク増加)
・両親の双極性障害罹患歴がある場合、ない場合と比較して、双極性障害移行リスク(調整後ハザード比)は約5倍となった。
・両親に精神病障害の罹患歴がある場合、ない場合と比較して、精神病性障害移行リスクは1.63倍となった
・両親の罹患歴がある場合には、双極性障害移行群、精神病性障害移行群いずれもPRS得点が高かったが、PRS得点の違いを補正後も結果はほとんど影響を受けなかった
・全体として単極性うつ病から双極性障害への移行の絶対リスクは7.3%、精神病性障害の移行リスクは13.8%であった
・PRSの四分位数毎の双極性障害への移行の絶対リスクの増加は約0.5%。精神病性障害への移行の絶対リスクの増加は約1%
・双極性障害のPRSsの上位1%の双極性障害移行の絶対リスクは9.1%、下位1%の移行リスクは5.7%、統合失調症のPRSsの上位1%の双極性障害以降の絶対リスクは16.2%、下位1%の移行リスクは11.6%
・両親の双極性障害罹患歴があり、双極性障害のPRSsが上位1%の患者については、双極性障害移行の絶対リスクが40.8%、一方で両親の双極性障害罹患歴があり、双極性障害のPRSsが下位25%の患者については、双極性障害移行の絶対リスクは26.2%であった。両親の罹患歴がなく、双極性障害のPRSsが下位25%にある患者については双極性障害移行の絶対リスクは5.6% であった
・両親の精神病性障害罹患歴があり、統合失調症のPRSsが上位1%の患者については、精神病性障害移行の絶対リスクは25.9%であり、統合失調症のPRSsが下位25%の患者については、精神病性障害の移行リスクは19.1%。両親の精神病性障害罹患歴がなく、統合失調症のPRSsが下位25%にある患者は、精神病性障害移行リスクは11.6%
・単極性うつ病患者について、双極性障害および統合失調症のPolygenic riskはその後の双極性障害および精神病性障害への移行リスクと有意な相関を示した
遺伝的要因が部分的にその後の双極性障害ないし精神病への進展リスクに関連していることとなる・PRSよりも両親の罹患歴の方が、特に双極性障害については、はるかに強力な予測因子となった。両親の罹患歴とPRSを組み合わせることで、さらに予測精度を向上させることができる可能性はある
・本研究は病院でのケアを受けた患者(全体の約25%)が対象であり、診療所やGPでケアされているうつ病患者は対象となっていない。そのため軽躁状態や軽度の精神病症状などは探知できていない可能性があり、PRSと進展リスクの関連を過小評価している可能性がある
・また両親の罹患歴による影響はPRSによる補正後もほとんど変化がないことから、両親の罹患歴による遺伝的ないし非遺伝的影響は、レアバリアント、コピー数多型、遺伝子間相互作用などの遺伝的要因や、親が罹患者であることによる早期受診、早期発見などの影響に起因するものであり、これらが将来の双極性障害発症や、精神病性障害発症リスクに大きく関与している可能性がある。
引用文献
1)Cathryn M. Lewis et al. Polygenic risk scores: from research tools to clinical instruments Lewis and Vassos Genome Medicine (2020) 12:44
2)AJP in Advance (doi: 10.1176/appi.ajp.2020.19111195)
3)Patterns and predictors of conversion to bipolar disorder in 91,587 individuals diagnosed with unipolar depression Acta Psychiatr Scand. 2018 May;137(5):422-432
4)Acta Psychiatr Scand . 2017 Apr;135(4):273-284




