-
PROTECT
2022年03月12日
・ICD-11からはゲーム障害(ゲーム症)が依存症の仲間入りするようで、DSM-Vでも研究用のカテゴリーですが、インターネットゲーム障害という診断名が登場しています。
・今回、インターネットゲーム障害に対して、PROTECTと呼ばれる認知行動療法的介入について、どの程度予防効果があるかについての介入試験結果が報告されました(文献1)
・PROTECTは思春期(12歳から18歳)におけるインターネット使用障害に対して開発された心理療法で、主に3つの領域における非適応的対処がインターネット使用障害の病態と強く関連すると仮定するものです。1つ目の問題が動機づけの問題や退屈に対する感受性の問題、2つ目の問題が不快な作業の先延ばしと関連する成果への不安、3つ目の問題が社会的スキルの欠如とそれに伴う社交不安になります。これら問題と向き合うことなく、インターネットにのめりこむことで、問題の先送りをしたり、問題から回避することで、より不安や不適応が増悪し、問題が大きくなるという仮説の下で介入が行われます。1つ1つの病態仮説に対して、それぞれの問題を抱える同世代の生徒が主役の物語を提示し、グループで話し合うことで問題点を自分たちのこととして捉え、よりスムーズに介入が進むように構成されています。PROTECTでは非適応的反応を4つのモジュールで修正していきます。
・4つのモジュールにおいて、認知再構成、問題解決技法、行動活性化、マインドフルネスの技法など様々な技法が取り入れられているのが特徴です。
思春期のゲーム障害と特定不能のインターネット使用障害のためのCBTに基づく介入
背景
・ICD-11では物質関連依存症と非物質関連依存症は神経生物学的に類似しているため、 “物質使用または依存行動による障害 ”に分類された
・ゲーム症(ゲーム障害)は、ICD-10では衝動制御障害に含まれていたギャンブル障害に加えて、新規の非物質関連依存症としてICD-11に記載された。インターネット使用障害など、その他の依存症は、依存症的行動に起因する「その他の特定の」または「特定不能の」障害として含めることが推奨されている。
・疫学研究ではゲーム症の有病率は4.6%、インターネット使用障害の有病率は6.0%と報告されている。特に、青年期は報酬系に関連する障害を発症しやすいと考えられている
・ 今回、ゲーム障害および特定不能のインターネット使用障害に対するPROTECTの長期的予防効果についてのクラスター無作為化比較試験を実施した
対象と方法
・ドイツのライン=ネッカー広域連合の全高校に校長室経由で連絡し、33校の高校が任意で参加した。データは2015年10月1日から2018年9月30日の間に収集された
・ゲーム障害と特定不能のインターネット使用障害のリスク評価のためのスクリーニングにCIUS( Compulsive Internet Use Scale )が使用され、20点をカットオフとして、中リスク以上の参加者(全スクリーニング対象者の上位36.4%に相当)が組み入れられた
・参加者は、ベースライン、1ヶ月時点、4ヶ月時点、12ヶ月時点で評価され、症状の重症度が評価された。また12ヵ月時点で依存症発症の有無を面接調査された
・PROTECTは、学校ベースの、マニュアル化された、認知行動療法に基づく予防グループ介入である。介入は、訓練を受けた心理士によって通常の学校時間内に実施。1回90分のセッションを4回実施。
・性別、年齢、学校の種類、成績、過去1か月以内の病欠、および平均オンライン使用時間も評価
・主要評価項目は、CSASで評価したゲーム障害または特定不能のインターネット利用障害の症状重症度(スコア範囲:0~56、スコアが高いほど病的)
・構造化臨床面接を用いて、ゲーム障害または特定不能のインターネット使用障害(DSM-5のインターネットゲーム障害の診断基準を5つ満たすと定義)および閾値以下のゲーム障害または特定不能のインターネット使用障害(DSM-5の診断基準を3つ満たすと定義)の発症率を調査
・副次評価項目は、先延ばし、一般精神病理、抑うつ症状、社会不安、パフォーマンス不安・学校不安、感情調節、学校関連社会行動・学習行動、自己効力感など
*PROTECTとは
・12-18歳の思春期層に対して開発された介入方法
・インターネットとビデオゲームの使用頻度の高くインターネット使用障害発症リスクのある全ての青年に適応可能
・DSM-V研究用試案におけるインターネットゲーム障害は過去12カ月間に以下の9項目中5項目以上が存在する場合に診断される
(1)ゲームへの熱中(ゲームをしていない時間にもゲームのことばかり考える。ゲームのために生活を組み立てる)(2)ゲームをしないと離脱症状が出現する(ゲームができない、もしくはやめようとすると抑うつ、不安、怒りなどを感じる)(3)耐性(ゲームへの欲求が増して、よりゲームに費やす時間が増大する)(4)ゲームをやめようとしても不成功に終わる(抑制コントロールの喪失)(5)他のレクリエーションへの興味を喪失する(社会的活動に不参加となりしばしば孤立する)(6)心理的問題があるにも関わらずゲームを続ける(社会的に有害な作用があるがゲームを継続する)(7)ゲームに費やす時間を他者に偽る(8)ゲームを現実生活の問題やネガティブな気分から逃避するために使用する(9)ゲームのため重要な対人関係や仕事、教育機会を喪失したりその危険がある・インターネット使用障害は、2つの強化メカニズムの結果として発症すると考える。第一のメカニズム(満足)は、インターネットが高い報酬をもたらすと認識され、インターネットの使用を繰り返し、増加させることにつながる場合に強化される。第二のメカニズム(補償)は、インターネット利用を優先する結果、運動、社会活動、学業、芸術、個人的に重要なプロジェクト、奉仕活動、自然に関する活動など、通常気分に強い影響を与える健全な活動がおろそかになることで強化される。これらの健全な活動は、青年期の感情制御の発達に重要なものである。現実世界でこのような体験を欠如することがインターネット使用への傾倒をもたらす
・PROTECT病因モデルは、思春期のインターネット使用障害が、主に3つの問題領域における否定的感情の不適応的対処と強く関連していると仮定する。これらは、(1)動機づけの問題または退屈への感受性の問題、(2)不快なタスクの先延ばしと関連する成果への不安、(3)社会的スキルの欠如とそれに伴う社交不安である。これらの状態は、思春期のインターネット使用障害に関連する危険因子であることが分かっている
Module 1:退屈と動機付けの問題
・現実世界とインターネット世界の良い点、悪い点を考える。これによりインターネットの利益と有害性についての知識を獲得することを目指す
・バランスを保つ:母親の食事の勧めを無視しSNSに熱中し、その後もネットゲームに熱中して親友の誕生日を忘れてしまうTONIの症例が提示される。この症例を通じて、TONIが現実世界とインターネット世界とのバランスのとれた生活をしているかどうかグループで議論する
・悪循環について考える:TONIがインターネットに多くの時間を費やすようになったのは、どのような負の感情のせいかを考える。あるいはコンピュータゲームをした後に、どのような肯定的な感情を経験するかを考える。最後に、TONIの過度のインターネット利用がもたらす長期的な否定的影響について考察する(母親とトラブルになる、パーティーに参加できない、サッカーの練習に付き合うかどうか聞かれなくなる、無気力になる、新しいことに挑戦する意欲がなくなる、友人/仲間や家族との連絡が減るなど)。インターネットは、これらの否定的な結果によって引き起こされる不快な感情を調整するための短期的な戦略として機能することが説明される
・続いて、認知が感情や行動に影響を与えることを学ぶ。非現実的な認知があれば、それを認知再構成し再評価する作業を行う。この過程をPROTECTでは”reality check”と呼ぶ。状況に対する推論の誤りが怒りや恐れなどの否定的な感情につながることを認識する
・思春期にみられやすい推論の誤りとして、“must thoughts(べき思考)”、または“demandingness (要求性思考)”がある。要求性思考とは、自分にも他人にも非現実的な要求を突きつけるもので、誰もそれを満たすことはできないものである。TONIの物語の中で、要求性思考に伴う機能不全のパターンを取り上げる作業を行う。セラピストはTONIの物語において、「これらの考え方はTONIの役に立つのか」かどうかを問いかける。生産的ではない役に立たない思考をセラピストは抽出していき、それらの思考が怒りや抑うつにつながることをみていく
・続いて「より現実的で役に立ち、TONIの気分を良くするような代替思考は何でしょう」と問いかけ、適応的思考について考え、認知の再構成を行っていく
・思考停止法について指導する:時には、あまりに不快な考えが浮かんできて、それに激しい感情で反応することがある。そんなときには思考停止法で対処する。思考停止法は、落ち込むような考えに対して自己主張するための手軽な方法で、自分に言い聞かせるだけでよい。こんなことを考え続けるのは嫌だ!と。現実でも内面でも、大きな声で「ストップ!」と叫んでみる。交通標識のようなものを思い浮かべて、思考を停止させることもできる。また、テーブルを手でたたいたり、足を軽くたたいたりして、思考から距離を置いてもよい。その後よりポジティブなことを考えたり、楽しい活動に没頭するようにする
・問題解決技法と行動活性化トレーニング:行動に直接介入する。問題解決技法を用いて行動変容を図る。まずは現在の行動パターンを分析する。退屈して何もする気が起きないのはどのような状況か、退屈をしないのはどのような状況かなど。続いて、非適応的な行動の代替となる行動にはどのようなものがあるかを考える。その代替行動のメリット、デメリットをリストアップし、最も適切な代替行動を選択し“change plan”を作成する。またchange planを実行できた場合に、自分に与えるご褒美を考える(自分自身のchange planを作成することが宿題となる)
Module 2:成果への不安と先延ばし
・まず「イライラするDavid」という症例が提示される。Davidは1週間後に数学のテストがあり、そのテスト範囲を1週間では理解できないと思っている。そして失敗への大きな不安を抱える。また良い成績をとらないといけないと考えている。テストに失敗すると考えると数学の授業も怖くなってしまう。イライラして帰宅したDavidはインターネットをはじめ時間を忘れて入り込んでしまう。その後数学の教科書を見ると罪悪感、嘔気を感じる。そのため再びインターネットを始めてしまう。Davidは数学のことをすっかり忘れてしまう。
・Davidがインターネットをすることについて、現実世界とインターネット世界とのバランスのとれた生活をしているかどうかグループで議論する。インターネット使用障害に典型的に見られる機能的および機能不全的な認知と行動を特定し評価する。この不適切な行動パターンと思考が現実世界とインターネット世界のアンバランスにどのように寄与しているかを議論する
・続いてDavidの症例で、退屈しのぎの悪循環について、Davidがどう考えるか、正の思考、負の思考を考える。また短期的、長期的な否定的な結果を予測する。インターネットの機能不全的な使用は、否定的な現実世界と肯定的な仮想世界という長期的な二項対立をもたらし、先送りや回避行動が恐怖を引き起こし、ますます強い抵抗につながることを学ぶ
・続いて、先延ばしを減らし、悪循環を断ち切ることを考える。先延ばしにすればするほど、しなくてはならないことから遠ざかり、さらにしたくない仕事をするよりも、他のこと(ゲームなど)を先にしなくてはならないという誤った信念の形成につながりうることを学ぶ。もっとも簡単な解決法は、したくない仕事への嫌悪感が益々増悪する前に、その嫌な仕事に取り掛かることである。仕事が終わったら自分自身にご褒美を準備する
・成果への不安についても同様に、物事に対して恐れを感じると(Davidのテストのように)、それを遠ざけようとしてしまい、遠ざけるとそのことが益々恐怖に感じるようになる。この恐怖を取り除く唯一の方法は、その対象に直面することである。それにより不安を生じる状況に速やかに対処すべきである
・続いてDavidの症例について、「べき思考」や「過度な一般化」などの認知のゆがみについて検討する。セラピストはDavidの物語において、「これらの考え方はDavidの役に立つのか」かどうかを問いかける。生産的ではない役に立たない思考をセラピストは抽出していき、それらの思考が怒りや抑うつにつながることをみていく。さらにより適応的な、現実的な思考はどのようなものかについて考える。
・最後にDavidの症例について問題解決技法を用いて行動変容を図ることを考える。まずは現在の行動パターンを分析する。インターネットをするのはどのような状況でどのような問題があるか、インターネットをすることの代替となる行動にはどのようなものがあるかを考える。その代替行動のメリット、デメリットをリストアップし、最も適切な代替行動を選択し“change plan”を作成する。またchange planを実行できた場合に、自分に与えるご褒美を考える(自分自身が先延ばしをすることについてchange planを作成することが宿題となる)
Module 3:社交不安
・まず一緒にプールに行く友達を探すがうまくいかないLeilaの症例が提示される。
・Leilaがインターネットをすることについて、現実世界とインターネット世界とのバランスのとれた生活をしているかどうかグループで議論する
・続いてLeilaがインターネットに多くの時間を費やすようになった不快な感情と、ネットでチャットをした後に感じる快感について考える。さらにインターネットを長時間使用することによって生じる長期的な否定的結果について考える(本当の友人がいない、他者に近づく方法を学ばない、他者に排除される、本当の友人のために努力する動機が少ない、自己効力感、自尊心が低下するなど)
・社交能力(social competence)のトレーニング:初対面の人に声をかけるときに、感じる不安や恐怖、ぎこちない態度は相手に伝わる可能性があるため、誰かと話をする前に、何を言いたいか考えておく。話しかけるのに適したタイミングを待つ。話すときは、はっきりと話す、さらに、常に相手に話す機会を与え、相手の話を遮ることなく、最後まで話させるなどの会話技法についてトレーニングする
・Leilaの症例について認知のゆがみを検討する。「べき思考」や「皆が」「いつも」「誰も~ない」などの思考や、「破局的思考」について検討する。これらの思考が現実的かどうかを考え、さらにより適応的な、現実的な思考はどのようなものかについて考える。
・最後にLeilaの症例について問題解決技法を用いて行動変容を図ることを考える。まずは現在の行動パターンを分析する。どのような行動が社交場面での危機や回避につながっているか、どのような行動をとればより安全に他者にアプローチできるかを考える。その代替行動のメリット、デメリットをリストアップし、最も適切な代替行動を選択し“change plan”を作成する。またchange planを実行できた場合に、自分に与えるご褒美を考える(自分自身が回避をすることについてchange planを作成することが宿題となる)Module 4:感情制御
・感情の星とよばれる図を提示し、自身の感情状態をセルフモニタリングするトレーニングを行う
・感情体験がいかに多面的で状況に左右されやすいかを視覚化する
・感情には4つの側面があり、1つは感情の認知的側面、2つ目は感情の生理的側面、3つ目は感情によって生起する気持ち、4つ目は気持ちにより生じる行動の側面であり、自身がどの状態にあり、それがどのような感情に起因するのかを同定することが目標
・マインドフルネスの技法に基づくもので、自身の体、知覚などに注意を向ける
・これまでのmoduleでみた3つのストーリーの主人公について、自身がその主人公であるとなりきって、行動の背景にある感情を探る
・感情は、ある状況下で適切な行動を示すために有用であり、出来事に対する適切な反応に寄与する特定の行動を活性化する要素を持っている。各感情の具体的な機能に焦点をあて、感情の星の外側に書き留める。例えば恐怖なら「自身を守る」など
・その後3つのリラクゼーション技法を導入し、感情制御の訓練を行う。具体的には「内なる安全な場所」「漸進的筋リラクゼーション」「熊のグミ」の3つの技法についてトレーニングを行う。
結果
・合計422人のリスクのある生徒(平均15.1歳、女性229人、男性193人)が、PROTECT介入群(n = 167)または評価のみの対照群(n = 255)に無作為割付
・介入は、3~11人から成る24のグループで実施。平均出席セッション数は、4セッション中3.7であった
・PROTECT介入群では、ゲーム障害と特定不能のインターネット利用障害の症状重症度が、対照群と比較して有意に低下した
・12カ月間の症状改善度はPROTECT群 39.8%、対照群 27.7%で効果量cohen d=0.67
・合計12人(5.7%)が、12か月後にDSM-5診断基準を少なくとも5つ満たす、特定不能のインターネット使用障害を発症した(PROTECT群6人、対照群6人)。
・合計40人(19.0%)がインターネットゲーム障害のDSM-5診断基準を3または4つ満たす閾値以下のゲーム障害(合計10人[PROTECT群3人,対照群7人])または特定不能のインターネット使用障害(合計33人[PROTECT群10人,対照群23人])に該当した(両方を満たすのが3名)
・発症率に有意差なし
・副次評価項目では、PROTECT介入群では、評価のみの対照群と比較して、先延ばしの減少が著しく大きいことがわかった。
・その他の副次評価項目では時間×群の交互作用は有意ではなかった
議論
・PROTECTは12カ月間でゲーム障害または特定不能のインターネット使用障害の症状の重症度を対照群と比較して有意に低下させた。一方で対照群における自然経過による症状軽減も大きかった。
コメント
・最初に4回のセッションを行い、その後1年間の経過観察期間での症状変化でみたものですが、途中でBooster sessionのようなものがあれば、1年後の発症率も違いが出たかもしれません
引用文献
文献1:Lindenberg K et al. JAMA Netw Open. 2022 Feb 1;5(2):e2148995. doi: 10.1001/jamanetworkopen.2021.48995.
-
抗精神病薬の減量について
2022年03月02日
・抗精神病薬をどのように減量するかについては様々な報告があり、鳥取医療センター(当時)の助川先生らの報告されたSCAP法(文献1)などが良く知られていますが、離脱症状や再発リスクを最小化することを目的として、D2受容体の占有率に基づく減量方法が提案されました(文献2)
・この論文に出会ったのは、最近でた抗精神病薬中止後の有害事象に関するメタ解析の論文(文献3)に引用されていたことに起因します。
・文献3では、どこかに過感受性精神病の証拠になるようなデータがないか、探してみたのですが、残念ながら直接的な証拠に出会うことはできませんでした。そもそも中止前の抗精神病薬のCP換算がわからないので、中止前にD2受容体の過感受性が形成されていたのかもわからないのですが、中止後の陽性症状の悪化やジスキネジアなどは有害事象としてほとんどみられないものでした(唯一ハロペリドール中止後の精神病症状出現がわずかに継続群と比較して有意差あり。しかし105名中4名にみられたのみ)。
・ドパミン過感受性による陽性症状再燃が存在するという主張に対して現状エビデンスが乏しいとするBPAガイドラインを書き換えるほどの証拠は見つかりませんでした。有害事象として不安が比較的多くみられていましたが、コリン離脱やアドレナリン離脱でも生じうるため、D2離脱によるものだけではないと思われます。
・Horowitzらが提案したのは、一定用量毎の減量(下図左)ではなく、下図右のようにD2受容体占有率の変化量が一定となるように減量する方法です(Schizophr Bull. 2021 Jul 8;47(4):1116-1129.より引用)。
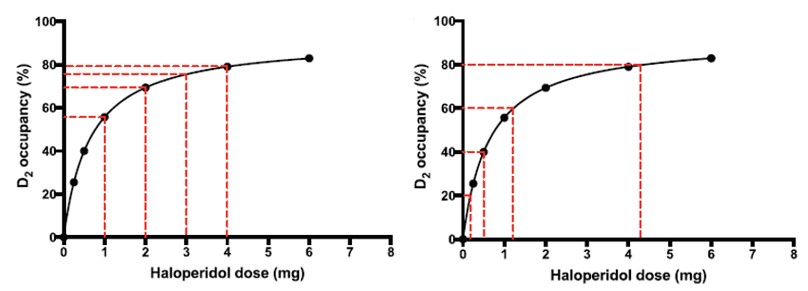
・また減量にかける時間も、遅発性ジスキネジアの寛解まで2-3年かかることから、長期投与中の患者については、全体でこのくらいの時間かけて漸減するのが妥当ではないかと提案しています。
・D2占有率の変化量をなるべく一定に保つための減量法として、直近の用量の25-50%(D2受容体占有率の変化量にして5-10%の変化割合に相当)を3-6か月毎に減量する方法や、直近の用量の10%ずつを1か月ごとに減量する方法などが挙げられています。
・また、クロザピンやクエチアピンのように、半減期の短かかったり、D2受容体からの解離が速いとされる薬剤では、より注意が必要で、個々の反応に応じて6-12週間ごとにD2(またはコリン受容体、ヒスタミン受容体)占有率を2.5-5%ずつ減量することが提案されています。
・この方法だと、高用量域では割と思い切った減量が可能な一方で、特に低用量域においては慎重な減量が求められることになります。果たしてSCAP法と比較して有害事象の発生率に差があるのか、興味深いところです。
文献1:Sukegawa T, et al: Study protocol: safety correction of high dose antipsychotic polypharmacy in Japan. BMC Psychiatry 14:103, 2014.
文献2:Mark Abie Horowitz et al. Schizophr Bull. 2021 Jul 8;47(4):1116-1129. doi: 10.1093/schbul/sbab017.
文献3:Lancet Psychiatry. 2022 Mar;9(3):232-242. doi: 10.1016/S2215-0366(22)00014-1. -
自閉スペクトラム症と腸内細菌
2022年02月22日
・以前腸内細菌のことを懇話会などで話題にしたこともあったので、まとめておきたいと思い時間がたってしまいました。
・特に自閉スペクトラム症(ASD)に対する糞便移植の結果についての報告(文献1)などは驚異的な結果で、オープン試験なのでエビデンスとしての質は低いものの、ほんとならすごいことだと思っていたのですが、今回の結果は、少し冷静になるべきかもしれない結果となります。(糞便移植自体は、ESBL産生大腸菌による死亡例の報告もあるので、慎重にすべきことになります)
・今回扱うのは2021年11月にCell誌に掲載された自閉スペクトラム症と腸内細菌の論文です(文献2)。なんとなく違和感を感じながら読んでいたのですが、その理由は横断研究なのに因果関係にまで言及されているからだと思います(例えば結果のところの表題でBehavior and preferences are upstream of reduced dietary and taxonomic diversityと表現されているなど)。この研究は横断研究なので、相関関係は議論できますが、因果関係については確定的なことは言えません。それなのに因果関係の議論についてかなり力が入っていて(著者らは仮説として慎重に扱ってはいますが)、表現を気をつけないとその話が独り歩きしてしまいかねません。横断研究の中で、因果関係を見出すためのいろいろな工夫がなされていることはわかるのですが、もうちょい慎重な書き方をされてもよかったのかなと思います。Behavior and preferences may be upstream of reduced dietary and taxonomic diversityくらいの表現でもよかったのではと思います。
・論文のFigure 4Jなどをみると、まるで自閉スペクトラム症の特性に起因した食事内容の偏りが腸内細菌叢の多様性の減少につながるかのようなモデルが提示してありますが、あくまで1つの仮説が提示してあるだけであり、この論文から結論付けられることではありません。正しいかもしれませんが、モデルの検証のためにはやはり前向き研究、できれば介入研究を行う必要があると思います。
・その点を踏まえても、これまでの大半の腸内細菌研究と異なり、細菌種のみを特定する16SrRNA解析ではなく、存在する腸内微生物(ウイルスも含む)の全ゲノム配列を調べるメタゲノムシークエンシングを行った点などはCell誌に掲載される価値のあった点になるのではないかと思います。
・文献2の概略ですが、オーストラリアの双生児プロジェクトなどに登録されたASD患者などを対象に、食事データ、便性状の一貫性、心理学的特徴、SNP遺伝子型などの共変量を用いて、腸内細菌叢の特徴を抽出しました。腸内微生物の同定にこれまでの16S rRNAシークエンシングとは異なり、メタゲノミクスシークエンシングを用いた点が異なります。
・対象となったのは自閉スペクトラム症と診断された99人(ASD群)、ASD診断のない同胞対照群51人(SIB群)、ASD診断のない同胞関係のない対照群97人(UNR群)の合計247人(2-17歳)でした。
・食事については、摂取記録から、3種類のPC値(PC1、PC2、PC3)が算出(PC1値が高いと植物性食品(野菜、果物、代替タンパク質)を多く含み、肉以外の非中核食品(甘い飲み物、スナック、焼き菓子、脂肪分の多い肉など)をあまり含まない食事と関連。PC2値が高いと、乳製品が多く、穀物が少ない食事と関連。PC3値が高いと、肉(脂肪の多い肉を含む)が多く、穀物や乳製品が少ない食事と関連)されました。便性状はブリストル・スケールで評価され、一塩基多型(SNP)より、ASDに関連したpolygenic risk scoreおよび神経症傾向に関連したpolygenic risk scoreが算出されました。
・便はティースプーン大の便サンプルを、おむつから掻き出すか、便器に吊るした器具から自宅で親が採取し、4mL RNAlaterに懸濁させたサンプルをクリニックに持参。便よりDNAを抽出し、Microba Genome Databaseを用いて微生物の種類が同定されました。
・分散成分分析により各共変量のb2値が算出(b2が大きいほど、その要因の寄与率が大きい)されました。このb2値を用いて、各共変量がどのASD診断などに寄与しているかが推定されています。
・結果ですが、腸内細菌叢の構成は自閉スペクトラム症診断に関して有意な相関があるとの結果は得られませんでした。それよりも腸内細菌叢構成は年齢や便性状、食事内容と有意な相関があることがわかりました。
・607種の腸内細菌の種について、ASD群とSIB群+UNR群の複合群(共変量:年齢、性別、食事PC1-3)で比較すると、Romboutsia timonensisという種のみがASD群で有意に低存在でした。
・これまでにASDとの関連が報告されてきたプレボテラ属、ファーミキューテス門、クロストリジウム属クラスター、ビフィドバクテリウムの種で有意な群間差は再現できませんでした。
・分散成分分析では、食品がASD診断と強い関連を有していました(b2=14%)。ASD群では、PC3値がSIB群およびUNR群より低く、肉類摂取が少ないことを示唆する結果でした。Shannon指数で評価した食事内容の多様性についてもASD群は有意に乏しいことがわかりました。
・食事と腸内細菌叢の多様性の間には有意な正の相関が見られました。相互回帰分析では、食事と腸内細菌叢の多様性は、互いの有意な予測因子でした。さらに、食事多様性回帰における最大の効果は群(SIB群、UNR群)からのものであり、一方、腸内細菌叢の多様性は群と関連していませんでした。このことから、ASDに伴う食事の偏りが、腸内細菌叢の多様性の低下と関連する可能性が示唆されました(あくまで可能性のみ。横断的研究の限界)
コメント
・興味深かったのは、figure 2より睡眠について、食事内容が有意な相関があるようにみえることでした。この点については論文中では触れてありませんでしたが、小児の睡眠について食事が重要であることを示唆する結果とはいえないのか、気になるところでした。・いずれにせよ、現在進行中の介入試験(NCT03408886、NCT04182633)の結果を待ちたいと思います。
文献1:Dae-Wook Kang et al. Sci Rep. 2019 Apr 9;9(1):5821. doi: 10.1038/s41598-019-42183-0
文献2:Chloe X. Yap et al., Cell. 2021 Nov 24;184(24):5916-5931.e17. doi: 10.1016/j.cell.2021.10.015. Epub 2021 Nov 11. -
寝るとやせるのか
2022年02月16日
・もともと睡眠時間が少なめで過体重気味の人が睡眠時間を増やすとどうなるかという短期的な介入試験の結果がJAMA Internal Medicine誌に公表されました(文献1)
・一番興味があったのは、どうやって睡眠時間を増やしたのかということでしたが、1時間程度のカウンセリングで、個別のライフスタイルに合わせた睡眠衛生指導をして、平日と休日における習慣的な睡眠・覚醒スケジュール、昼寝(ある場合)、環境要因(寝室の温度、騒音、環境光)、就寝時の習慣、テレビ・電子機器の使用、生理的要因(例:運動、カフェイン)などが検討され、就寝時間を8.5時間に延長することを目標に、2週間自宅で行う就寝・起床時間のスケジュールが個別に提供されたとのことです。要は自分の生活スタイルをきちんと見直して、睡眠を確保できる時間を作り出しましょうということになります。
過体重に対する睡眠延長効果
背景
・米国人口の3分の1は、推奨される7~9時間の睡眠をとっていない。定期的な睡眠時間が7時間未満であることは、健康への悪影響と関連することが報告されている。・前向き観察研究により、睡眠時間の短さは体重増加の危険因子であることが報告されている(JAMA Intern Med. 2020;180(12):1694- 1696)。しかし、睡眠時間の延長が肥満の予防や改善に有効であるかどうかはわかっていない。
・エネルギー摂取量が100kcal/日持続的に増加すると、3年間で約4.5kgの体重増加をもたらすとされている
・実験室での短期的な研究では、健康な人の睡眠を制限すると、エネルギー消費量はほとんど変化せず、平均エネルギー摂取量が約250〜350kcal/日増加することが報告されている(Sleep Med Rev. 2019;45:18-30)
・今回、習慣的に睡眠時間が短い過体重の成人を対象に、実生活の場で客観的に評価したエネルギー摂取量、エネルギー消費量、体重に対する睡眠延長介入の効果を明らかにするために、RCTを実施した
対象と方法
・21歳から40歳の成人男女で、BMIが25.0〜29.9、平均習慣的睡眠時間が一晩あたり6.5時間未満の人。・過去6ヶ月間、自己申告による睡眠習慣が安定していること。
・習慣的な睡眠時間は、自宅でのアクチグラフ検査(1週間)で確認。
・睡眠ポリグラフ検査で確認された閉塞性睡眠時無呼吸症候群(AHI>5)、不眠症または他の睡眠障害の既往、夜勤および交代制勤務(現在または過去2年間)を有する者は除外参加者は全員、ベースライン評価期間で2週間の習慣的睡眠をとり(この期間に習慣的な睡眠覚醒パターンを把握)、その後2週間の睡眠延長(睡眠延長群)または2週間の習慣的睡眠継続(対照群)のいずれかに無作為に割り付けられた。ベースライン評価期間中、参加者は、食事や身体活動を制限されることなく、自宅で日常的な活動を継続した。
・睡眠覚醒リズムは4週間の全期間中アクチグラフで評価
・睡眠延長群では、構造化面接により個別の睡眠衛生カウンセリングを受けた。面接の最後に、参加者は就寝時間を8時間半に延長する目的で2週間自宅で実行すべき個別の推奨事項を提示された。22日目(介入開始1週間後)にはフォローアップ訪問が実施された。アクチグラフでの睡眠データに応じて、さらなる睡眠カウンセリングが提供された。
・対照群では、15日目(介入開始時)と22日目に調査員と面会を実施。対照群のアクチグラフデータはダウンロードされたが、特に睡眠に関する指示を受けず、研究終了まで日常生活と習慣的な睡眠行動を継続するよう指示された
・総エネルギー消費量は二重標識水法で測定。
・2週間ごとに、体内エネルギー貯蔵量の変化を、毎日の体重測定と二重エネルギーX線吸収測定法による体組成(脂肪量と無脂肪量)の変化の回帰係数(傾き、グラム/日)から計算。
・参加者は毎朝起床後、飲食前に2回、裸体重を測定するように指示され、体重は、行動への影響を最小限にするため、参加者に隠蔽された。
・体組成の変化は、脂肪量のエネルギー係数を9.5 kcal/g、無脂肪量のエネルギー係数を1.0 kcal/gとして、貯蔵エネルギーの変化に換算した。
・安静時代謝量は、空腹時30分後と標準化した朝食後4時間の間接熱量測定により測定した。
・活動エネルギー消費量は、総エネルギー消費量から安静時代謝量と食事の熱効果を差し引くことで算出された。
結果
・対照群41人、睡眠延長群39人。平均年齢29.8歳、男性41人(51.3%)、女性39人(48.7%)
・睡眠延長群の参加者は、対照群の参加者と比較して平均睡眠時間がベースラインから有意に増加した(1.2時間;95%CI、1.0 -1.4時間)。参加者の勤務日(1.3時間;95%CI、1.0~1.5時間)または非勤務日(1.1時間;95%CI、0.7~1.5時間)いずれも有意に増加。
・睡眠効率の変化は2群間で有意差なし。
・エネルギー摂取量は、対照群と比較して睡眠延長群で有意に少なかった(-270.4 kcal/日;95% CI,-393.4 to -147.4 kcal/日)。
・対照群ではエネルギー摂取量がベースラインから有意に増加し(114.9 kcal/日;95%CI、29.6~200.2 kcal/日)、睡眠延長群ではエネルギー摂取量がベースラインから有意に減少した(-155.5 kcal/d;95%CI、-244.1~-66.9 kcal/d)
・すべての参加者を考慮すると、睡眠時間の変化はエネルギー摂取量の変化と逆相関していた(r = -0.41; 95% CI, -0.59 to -0.20)。睡眠時間が1時間増加するごとに、エネルギー摂取量は約162 kcal/日減少した(-162.3 kcal/日;95% CI,-246.8 to -77.7 kcal/日)。
・総エネルギー消費量やその他のエネルギー消費量の指標に、両群間の有意差なし。
・睡眠延長群では、対照群と比較して、体重が有意に減少(-0.87 kg; 95% CI, -1.39 to -0.35 kg)。
・対照群ではベースラインからの有意な体重増加(0.39 kg; 95% CI, 0.02 to 0.76 kg)があり、睡眠延長群ではベースラインからの有意な体重減少(-0.48 kg; 95% CI, -0.85 to -0.11 kg)がみられた
議論
・健康的な睡眠時間に延長することが、客観的に評価されたエネルギー摂取量および体重に有益な効果をもたらすことを示唆する結果が得られた。Hallの動的予測モデルによると、本試験で観察された約270kcal/日のエネルギー摂取量の減少は、その効果が長期的に持続した場合、3年間で約12kgの体重減少を予測する。これが続けられるかどうかはわからない
・一方でメタ解析では、健常者における1~14日間の短期睡眠制限は、平均エネルギー摂取量の約253kcal/日の増加と関連することが報告されている( Sleep Med Rev. 2019;45:18-30)。また別のメタ解析では、睡眠時間が1時間減少するごとに肥満リスクが9%増加することが報告されている(Sleep Breath. 2019;23 (4):1035-1045)
・睡眠延長群は対照群と比較して、十分な睡眠を得るという主観的スコアが有意に高く、日中のエネルギーと覚醒度が高まり、気分も良くなった
・健康な睡眠習慣は肥満および関連疾患の予防のためにも重要である
コメント
・対照群ではそのままの生活の継続なのになぜか消費カロリーが有意に増えてしまっているのがどういう理由なのか気になります。・ちなみにアクチグラフによる睡眠ないし覚醒の判定にはAW2式とCole式の2つの方法があるようですが、だいたいポリグラフとの睡眠覚醒判定の一致率は88%くらいのようです(文献2)
引用文献
文献1:Tasali E. et al. JAMA Intern Med. 2022 Feb 7. doi: 10.1001/jamainternmed.2021.8098. Online ahead of print.文献2:Cole R.J. et al. Sleep 1992;15(5):461-469
-
備忘録
・忘れないでおきたい小ネタをいくつか書き留めておきたいと思います。
診断分類の話とか
・診断カテゴリーの細かいことはなかなか覚えづらいのですが、専門医試験で聞かれることもあるみたいなので、無視もできないことになります。DSM-IVの身体醜形障害は身体表現性障害下に分類されていましたが、DSM-Vでは強迫症および関連症群下に分類されています。ICD-10では身体醜形障害は独立した病名として存在せず、身体表現性障害下の心気障害に含まれています。ICD-11では心気障害が心気症として強迫症または関連症群のカテゴリー下に移されました。またICD-11では身体醜形症として心気症から独立しました。適応障害はICD-11では適応反応症へ病名変更。このような変更点はまだまだたくさんあるのでまとめておこうかと思いましたが、気力がわきません。DSM-IV-TRで研修した身としては、病名の変更など、患者さんの利益にすぐにつながりにくいことについては、なかなかなじみにくいことではあります(多分専門が精神科以外の先生はもっと戸惑われると思います)
ALS plateauとreversal
・PRO-ACTデータベースには、様々な臨床試験におけるALSのデータが集積されており、それを用いて一定期間において進行が停止する(プラトーになる)もしくは改善(reversal)する割合がどの程度かについての報告(Neurology. 2016 Mar 1;86(9):808-12.)がありました。最近中国からの前向き観察研究の結果が報告(J Clin Neurosci. 2022 Jan 21;97:93-98)されたのですが、こちらの方が大規模データなので、小規模試験の結果を解釈する際に参考になるのでまとめておきます。特に10例程度の症例報告で一部に進行停止がみられたなどの報告がある場合に、その結果がどの程度確からしいのかについて批判的に吟味する際に役にたちそうです。
・PRO-ACTデータベースによると、ALSFRS-Rの変化量でみた場合、6カ月間では25%が進行せず(対象者数3132名)、12カ月では16%が進行せず(2105名中)、18カ月間では7%が進行しなかった(1218名中)。reversalについては、180日間で14%(1343名中)がALSFRS-Rの変化量が0を超えた(改善した)とのことです。。この結果に関する注意点は、PRO-ACTデータベースへの参加者で構成されており、主に無作為割付比較試験への参加者であるため、実際の患者層の状態変化を反映していない可能性がある点です。四肢発症型の118名を対象とした前向き観察研究(J Clin Neurosci. 2022 Jan 21;97:93-98)では、6カ月間でのreversalの割合が8.47%であり、3か月間でのプラトーの割合はだいたい20-25%程度と報告されています。これらの結果から得られることは、例えば10名を対象とした小規模試験を行う場合、この規模の試験ではそもそもが病気の進行について何か言える試験規模ではないのですが、予備的な結果として、6カ月間で5名が進行停止しましたという結果が得られた場合、非常に大雑把な検定をすると、統計的に有意な結果とはいえないということになります。
ADHD治療薬と物質乱用リスク
・ADHD治療薬、特に精神刺激薬(メチルフェニデートなど)と物質乱用リスクについてです。勉強会ではlancetの総説(Lancet. 2020 Feb 8;395(10222):450-462)を使ったりしていたのですが、その中において、精神刺激薬が物質乱用や依存の可能性を高めるかもしれないという懸念について、2014年の観察研究の報告(J Child Psychol Psychiatry. 2014 Aug;55(8):878-85.)が引用されていたのでまとめておきます。結論からいうと、3年程度の観察期間において、ADHD患者全体としては、非ADHD患者よりも物質乱用リスクは高かったものの、ADHD患者内で検討した場合、精神刺激薬を使用していた群は、使用していなかった群と比較して、物質乱用リスクは各種共変量(年齢、性別、服薬状況、精神疾患、社会経済状況など)についてCox回帰分析にて調整した結果、31%程度有意に低くなるとの結果でした。SSRIの使用の有無で物質乱用リスクを比較したところ、ハザード比は1.04と有意差はありませんでした。ADHD治療薬は犯罪率の減少にもつながりうるとの報告(N Engl J Med 2012; 367: 2006–14.)もあり、いずれも観察研究からの帰結ではありますが、長期的有益性を支持する結果といえそうです。しかし精神刺激薬については耐性などの問題もあり、その適応には慎重になる必要があります。
上市される割合はどのくらいか
・世界のバイオ技術関連企業などが設立した団体であるThe Biotechnology Innovation Organizationというところが、2011年から2020年までの臨床試験の成功率などを分野毎にまとめて公表しています(https://www.bio.org/clinical-development-success-rates-and-contributing-factors-2011-2020)。
・神経変性疾患領域でのここ最近の第3相試験の惨敗状況(NurOwn細胞やtofersen、レボシメンダン、aducanumabはさておき、その他の抗Aβ抗体、BACE阻害薬など)をみると、ここまで第3相からNDAに行く割合が高い(53.1%)とは思っておらず意外な数字でした。
・ここまで高い数字になっているのは、基礎から開発された薬剤のみならず、例えば注射薬の経口薬版とか(最近だとエダラボンの経口薬)の第3相試験も含んでいるからかなと思います。




