-
なんでネコなのか
2021年07月21日
・トキソプラズマは何でネコの腸管上皮でしか有性生殖ができないのか。そのナゾに対する答えがわかったのは割と最近のようです。
・文献1によれば、ネコは哺乳類の中で唯一、リノール酸の代謝に必要なデルタ-6-デサチュラーゼ活性を腸内で欠損しており、その結果、全身的にリノール酸が過剰になっているということです。腸管上皮でのリノール酸の存在が、トキソプラズマの有性生殖を可能にしているらしいとのことで、この報告ではマウスのデルタ-6-デサチュラーゼを阻害し、その食餌にリノール酸を加えることで、マウスで有性生殖が可能になることを示しています。
・というわけで本題ですが、文献2に健常者におけるトキソプラズマ感染と認知機能の関係についてのメタ解析結果が報告されました(文献2)。
健常者におけるトキソプラズマ感染と認知機能
背景
・トキソプラズマに感染した齧歯類は、非感染の齧歯類と比較して、危険を冒す行動や衝動的な行動を示すことがあり、感染したマウスは、反応速度の低下、学習能力の低下、運動能力の低下を示すことがあると報告されている
・ヒトにおいては、統合失調症、双極性障害、自殺リスク、交通事故リスクの増加などとの関連が報告されている
・トキソプラズマと統合失調症リスクについては、文献3において約18年間の縦断的なnested case-control 研究の結果が報告されている。
・この報告では、症例群としては18歳から65歳までの最近発症した精神病群(n=221、少なくとも中程度の重症度の陽性症状が数日間にわたって続く、もしくは週に数回発生するなどの頻度の精神病症状が過去24カ月以内に初めて発症した群)が設定され、抗トキソプラズマIgG抗体の陽性率が健常コントロール群(n=571)や慢性期の統合失調症患者(n=752)、双極性障害患者(n=444)、うつ病患者(n=64)などと比較された。
・最近発症した精神病群はDSM-IVにより精神病症状を伴う気分障害群と、統合失調症圏(統合失調症や統合失調感情障害など)に分類された。最近発症した精神病群の平均罹病期間は約1.3か月であり、慢性期の統合失調症群の平均罹病期間は約20年、慢性期の双極性障害群およびうつ病群では約17年であった。
・抗トキソプラズマIgG抗体は固相酵素免疫測定法で測定され、標準試料の0.8倍以上のシグナルが得られた場合に陽性と判定。
・抗トキソプラズマ抗体陽性の最近発症した精神病群のコントロール群に対する調整後オッズ比(就業年数、性別、人種、母親の学歴、出生地などで調整)は2.44で有意差あり。非気分障害圏の最近発症精神病群の調整後オッズ比は2.49、精神病症状を伴う気分障害群の調整後オッズ比は2.40でいずれも有意差ありであった。
・一方慢性期の統合失調症、双極性障害、うつ病についてはコントロール群と抗トキソプラズマ抗体陽性に関して調整後オッズ比は有意差がないとの結果であった。
・この結果については、次のように考察されている。つまり統合失調症については罹病期間が長くなり、かつ再暴露がないと、抗体濃度は時間とともに低下し、発症から何年も経つと対照群と変わらない抗体濃度になる可能性があること。また統合失調症や双極性障害の治療に用いられるバルプロ酸やその他の薬剤は、細胞培養において抗トキソプラズマ活性を持つことが示されており、これにより、時間の経過とともに抗トキソプラズマ抗体の血清陽性率が低下することにつながる可能性があるためではないかなどと考察されている。(しかしこの報告もトキソプラズマ感染歴や感染からの期間が評価されたわけではないため、この考察が正しいかどうかはわからない)
・今回、システマティックレビューとメタ解析を行い、健常者のトキソプラズマ血清反応陽性と認知機能低下との関連性を検討した
対象と方法
・健常者で血清抗トキソプラズマ抗体を測定され、認知機能が評価されている観察研究(横断的および縦断的)
・認知機能テストについては、処理速度、ワーキングメモリ、短期言語記憶、実効機能などに大別され、これら4つの領域でメタ解析が可能であった
結果
・13 studies(n=13289)がメタ解析の対象となった(うち3006名、22.6%が抗トキソプラズマ抗体陽性)
・処理速度(Trail Making Test A、Serial Reaction Time Test、go/no-go reaction time testのいずれかで評価)については9 studiesで評価。全体の効果量は0.12で有意差あり。Heterogeneietyの指標であるI^2は13%と低かった
・ワーキングメモリ(Wechsler Adult Intelligence Scale、Wechsler Intelligence Scale for Children digit span test measuringworking memoryなどで評価)については6 studiesが評価。SMD=0.16で有意差あり。Heterogeneiety I^2=0% 異質性なし
・短期言語記憶(Auditory Verbal Learning Test、California Verbal Learning Test、Verbal Learning and Memory Test measuring short-term verbal memoryなどで評価)は5 studiesで評価。SMD 0.18と有意差あり。Heterogeneiety I^2=22%でmoderate
・実効機能(Trail Making Test B、verbal fluency test、clock drawing testなどで評価)については8 studiesが評価
SMD 0.15で有意差あり Heterogeneiety I^2=63%で有意。ただし質の低いstudyを除外したsensitivity analysisでもSMD=0.15で有意差あり結論
・トキソプラズマ感染は評価した全ての認知領域において、小さいながらも有意な認知機能の悪化をもたらす可能性があるとの結果になった
・しかし、これらの関連性は主に横断研究(13 studies中9 studiesが横断研究で残りはコホート研究)から得られたものであるため、認知機能低下がトキソプラズマ感染と因果関係があるかどうかは明確ではない。逆因果関係(認知機能低下や精神医学的問題をより多く抱えている人は、より高い確率で感染する)や、トキソプラズマ感染と認知機能低下や精神医学的問題の両方の可能性を高める別の要因(例えば貧困、MMP-9遺伝子多型など)を排除することはできない
・今後は、縦断的研究を行い、社会経済的な状況、菌株の種類、血清濃度、考えられる複合感染(サイトメガロウイルスやヘルペスウイルスなど他の感染症との重複感染が免疫応答に影響することが知られている)、感染期間など、潜在的な交絡因子を検討することが必要となる
コメント
・妊娠中は垂直感染リスクがあるためネコ(特にフン)との接触や生肉や井戸水などの摂取を避ける、土壌に触れる際には手袋をするなどの感染防御策をとったほうがよさそうです。
文献1:Bruno Martorelli Di Genova et al. PLoS Biol. 2019 Aug 20;17(8):e3000364. doi: 10.1371/journal.pbio.3000364. eCollection 2019 Aug.
文献2:Lies de Haan et al. JAMA Psychiatry. 2021 Jul 14;e211590. doi: 10.1001/jamapsychiatry.2021.1590.
文献3:Yolken R et al. PLoS Negl Trop Dis. 2017;11:e0006040. -
ストレスチェックについて
2021年07月14日
・労働安全衛生法により従業員50人以上の事業所では義務化され、50人未満では努力義務とされるストレスチェック制度ですが、これはメンタルヘルス不全の一次予防のために使用することを意図して行われるものです。このことは厚労省も明記しています。
・とかく希望者による高ストレス者の面談が注目されがちなストレスチェック制度ですが、これは本来意図された使い方ではありません。高ストレス者については全体の10%が該当するように事前の大規模なテストで閾値が設定されており、職場全体に占める高ストレス者の割合のこの数値からどの程度乖離しているかも職場環境の1つの指標にはなりうるかと思われます。
・高ストレス者の面談といえば二次予防のように思われますが、ストレスチェック制度は二次予防目的ではないことに注意が必要で、むしろこれまでのエビデンスからは二次予防として使用してはならないと考えた方がよさそうです。
・一次予防として使用するとはどういう意味かというと、きちんと集団解析を行い、事業場の環境改善を行い、メンタルヘルス不全の発生しにくい職場づくりのために役立てなければ意味がないということです。
・もし集団解析を職場の環境改善に役立てていない事業所があれば、単にストレスチェックのための労力とお金を捨てているだけだと思われます。
・なぜこのようなことが言えるのかについて、これまでのエビデンスをみてみます。
・まずはうつのスクリーニングをして、その結果をプライマリケア医に伝えることが何らかの有益なアウトカムをもたらすのかどうか、メタ解析の結果(CMAJ 2008;178(8):997-1003)をみてみます。
・この結果には5つのstudyが含まれていますが、たとえばかなり症例数の多いLewisらの報告(Fam Pract. 1996;13:120-6)では、ロンドンのある診療所に通院する患者の中からエントリーされた681名の患者を対象に、12項目のGeneral Health Questionnaire (GHQ:2-3週間前から現在までの健康状態で、精神的・身体的問題があるかどうかのスクリーニング)を全員に行い、患者は3つの群に無作為割付されました。
・第1群はかかりつけ医に何も伝えない群、第2群はGHQ-12の結果のみを伝える群、第3軍はGHQ-12に加えてさらにコンピュータを用いた自己評価式の20分間ほどのPROQSYと呼ばれる精神的健康度に関するアセスメントを受け、その解析結果もかかりつけ医に伝えられ、かかりつけ医とその結果について議論する機会を持ったものとされました。
・そして、6週後、3か月後、6か月後のGHQの各群の平均点が比較されました。その結果、6週後においては第3群がわずかに有意にGHQ平均点が良好であったものの、3か月後、6か月後のGHQ得点は群間有意差なしとの結果でした。プライマリケア医にスクリーニング結果を伝えようが、伝えまいが、長期的な精神的健康度に関するアウトカムはほとんどかわらなかったということになります。
・類似したアウトカムを評価した介入試験は2008年時点で5つあり、そのメタ解析結果が下図です(引用元:Simon Gilbody DPhil et al. CMAJ 2008;178(8):997-1003)。
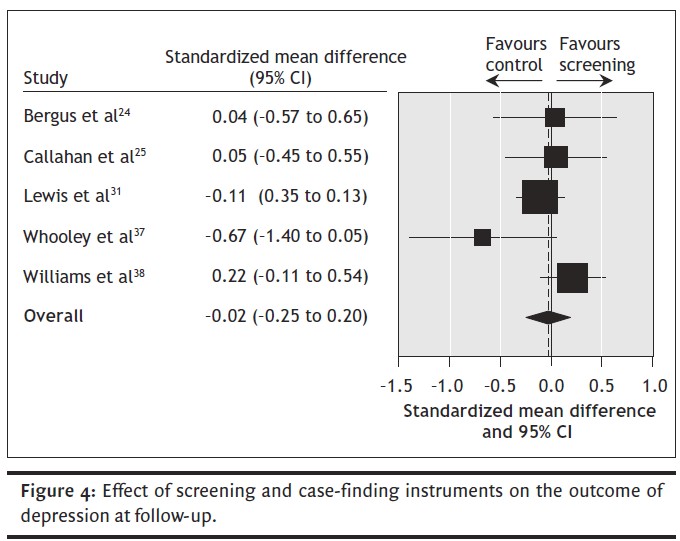
・残念ながら、精神的健康度に関するスクリーニングを行い(いくつかのstudyはうつ病に特化したスクリーニングを使用)、その結果をかかりつけ医に伝えようが、伝えまいが、3か月以上の長期的な精神的な健康度に関するアウトカムはかわらなさそう、ということがいえます。この状況はストレスチェックにおける面談にも似ていて、1度だけの面談で終わる場合、その結果について医師や健康管理スタッフと議論する機会があろうがなかろうが、長期的な精神的健康度についてのアウトカムはかわらない可能性があると言えます。ですので、厚労省は、ストレスチェックについては集団解析をして、環境改善をして一次予防に活用しなさいと言っているわけです。
・では、どうすれば、スクリーニングが意味を持つのか?それは、スクリーニングとケアを組み合わせた介入を行うことのようです。ケアも行うので、予後が良くなって当然のようにも思えますが、時間と労力はかなりのものになります。
・例えば文献1は、閾値下のうつ症状を有する患者を対象に、協同的ケア(collaborative care)と通常ケア(プライマリケア)を比較した介入試験になります。
閾値下うつ症状を有する高齢者のうつ症状に対する協同的ケアと通常ケアの比較
背景
・閾値下のうつ状態については、薬物療法は第1選択ではない。また認知行動療法や対人関係療法、行動活性化療法などの専門療法はより重篤なうつ状態に適応となることが多い・協同的ケア(collaborative care)は、訓練をうけたケアマネージャーらにより提供されるものである。イギリスにおいて、協同的ケアが閾値下のうつ状態に有用かどうかを介入試験により検証した
対象
・65歳以上のプライマリケア患者で、「過去1ヶ月間に気分の落ち込み、憂うつな気分、絶望感のいずれかで悩んでいますか」もしくは「過去1ヶ月間に興味の減退や喜びの感情の喪失により悩んでいますか」の質問のいずれかでyesであるもの
・さらに、訓練を受けた研究者による電話インタビューでDSM-IVの閾値下うつ病に該当するもの
・認知機能低下やアルコール依存などは除外
方法
・無作為割付single blind試験
・参加者は協同的ケア群(N=344)ないし通常のプライマリケア群(N=361)に割付
・協同的ケアは、メンタルヘルス専門看護師もしくは心理士資格を有するケアマネージャーにより提供。提供期間は8週間で、この間電話によるサポート、症状のモニタリング、行動活性化(うつ症状により失われた社会的活動や報酬探求的活動の活性化)のための構造化プログラムの提供などを行い、必要に応じてケアマネージャーは精神科医などによる助言を得た。
・主要評価項目は4か月時点でのPHQ-9得点(うつ症状尺度)
結果
・4か月時点でのPHQ-9得点は、協同的ケア群平均5.36点、通常ケア群 6.67点で有意差あり。
・4ヶ月時点でうつ病と診断されたものは、協同的ケア群 17.2%、通常ケア群 23.5%で有意差なし。12ヶ月時点でうつ病と診断されたものは、包括的ケア群 15.7%、通常ケア群 27.8%で有意差あり
・うつ症状尺度(PHQ-9)、不安症状尺度(GAD-7)については、4ヶ月時点、12ヶ月時点いずれも有意差あり
結論
・スクリーニング後の協同的ケアは閾値下うつの予後を改善する可能性がある
コメント
・ストレスチェック制度は義務化された事業場ではそれなりにコストや労力がかかっているものと思われます。単なるスクリーニングとして使用するのではなく、集団解析を行い、問題点を抽出し、職場環境改善を行って(たとえば、具体的な環境改善の方法としてはhttps://kokoro.mhlw.go.jp/manual/を参照)有効活用したいものです。
文献1:Gilbody S et al. JAMA. 2017 Feb 21;317(7):728-737.
-
亜酸化窒素(笑気)
2021年07月06日
・エスケタミンが2019年3月5日にFDAより治療抵抗性うつ病に対する抗うつ薬併用療法として承認されました。もともと麻酔薬として承認されているケタミンですが、NMDA受容体拮抗作用により抗うつ作用を発揮すると考えられています。その効果は投与開始2時間後から明らかで、速効性があると言われています(JAMA Psychiatry. 2018 Feb 1;75(2):139-148. )。
・NMDA受容体拮抗薬が抗うつ作用を有するかもしれないということは、すでに1990年頃からマウスの実験で言われていたようです(Molecular Psychiatry vol. 23, 801–811 (2018))。さらに各種抗うつ薬のマウスへの慢性投与によりNMDA受容体への放射性リガンドの結合が減少することが報告され、抗うつ薬慢性投与によりNMDA受容体の適応的変化が生じることが推測されていました。
・ケタミンは、健常者の前頭前野において神経活動を増加させることが示されていて、これはGABA作動性介在神経に発現しているNMDA受容体を優先的に阻害するためと考えられているようです。GABA介在神経の抑制による皮質活動の脱抑制が迅速な抗うつ作用発揮の要因との仮説も存在しますが、一方で、GABA介在神経の活動を賦活化するとマウスで抗うつ作用が観察されるなど、この仮説と矛盾する実験結果もあり、はっきりしたことはわからないというところのようです。
・NMDA受容体拮抗薬であるメマンチンとの違いについては以下のように説明されています。グルタミン酸神経のシナプスにおけるシナプス小胞グルタミン酸の自発的放出は、微小シナプス電流(mEPSC)をもたらし、この微小シナプス電流は蛋白質合成を抑制する働きを有するとのことです。ケタミンはNMDA受容体遮断により微小シナプス電流を抑制し、蛋白質合成の抑制を解除し、海馬CA1領域におけるシナプス増強を促進するなどして、抗うつ作用をもたらすことを示唆する結果が得られています。一方でメマンチンは非競合的なNMDA受容体遮断薬であり、微小シナプス電流を抑制しないため、抗うつ作用を発揮しないのではないかと考えられているようです(Molecular Psychiatry vol. 23, 801–811 (2018))
・また樹状突起などのシナプス外にもGluN2Bサブユニットを含むNMDA受容体が存在しており、このGluN2B-NMDA受容体が活性化するとmTORシグナル経路を介して、シナプス恒常性維持に関与する蛋白質合成が抑制されるとのことです。ケタミンはこのNMDA受容体を阻害し、蛋白質合成の抑制を解除し、これもまた抗うつ作用の発揮に関わっているのではないかとの仮説もあります。ただし、GluN2B-NMDA受容体拮抗薬であるMK-0657は第2相試験で抗うつ作用を確認できなかったことから(JAMA psychiatry. 2016; 73(7):651–652.)、これもまたはっきりしたことはわかりません。
・その他、NMDA受容体とは別のイオンチャネル型グルタミン酸受容体であるAMPA受容体もまたケタミンの抗うつ作用に関与していると言われており、ケタミン投与によるGABA介在神経の抑制を介したグルタミン酸神経系の活性化はAMPA受容体の活性化をもたらし、抗うつ作用の発揮に関連するとの仮説もあります。またケタミンは海馬TrkBのリン酸化を介してBDNF合成を促進し、NMDA受容体遮断を介してeEF2K経路を阻害することにより蛋白質合成を促進するなどし、抗うつ作用に寄与するとの仮説もあるようです。
・はっきりしたことはよくわからないケタミンの抗うつ作用ですが、今回笑気(亜酸化窒素)による治療抵抗性うつ病に対する第2相試験の報告がなされました(Sci Transl Med. 2021 Jun 9;13(597):eabe1376. doi: 10.1126/scitranslmed.abe1376.)。これまたNMDA受容体遮断作用を有する薬剤による報告となります。このような麻酔作用、催幻覚作用を有する薬剤の臨床試験における問題点も最後にコメントしておきます。
治療抵抗性うつに対する亜酸化窒素背景
・大うつ病の生涯有病率は約10-20%と推測されており、そのうつ少なくとも1/3の患者が治療抵抗性と考えられている・2015年に20名の治療抵抗性うつ病の患者を対象とした概念実証試験(プラセボ対照クロスオーバー試験:Biol. Psychiatry 78, 10–18 (2015))では、1時間の50%亜酸化窒素(50%笑気/50%酸素)はプラセボ(50%二酸化窒素/50%酸素)吸入群と比較して、吸入2時間後にHAM-D21の亜酸化窒素群とプラセボ群の点差は-4.8点、24時間後には-5.5点であり、亜酸化窒素吸入群が有意に良好な結果となった。亜酸化窒素はNMDA受容体拮抗作用を有し、ケタミンと類似した作用機序により抗うつ作用を発揮する可能性がある
・しかし亜酸化窒素50%には嘔気、嘔吐などの副作用の懸念があり(2015年の試験では15%に出現)、今回、より低濃度の亜酸化窒素(25%亜酸化窒素)で有効性があるかどうか、副作用が少ないかどうか、さらに治療効果が24時間以上継続するか、少なくとも14日間追跡を行った
方法と対象
・18-75歳までの大うつ病患者
・MADRSで19点以上
・過去に3回以上の適切な用量・期間の抗うつ薬治療に反応しなかった経験があり、かつ現在のエピソードにおいて1回以上の抗うつ薬治療に反応していない患者
・パーソナリティ障害、パニック症、双極性障害、統合失調症圏、物質使用障害は除外
・試験開始4週間前から投薬内容の変更はなく、また試験開始後3か月間も抗うつ薬の用量や内容の変更は行わないこと
・プラセボ対照二重盲検クロスオーバー試験
・患者に対してランダムな順序で50%亜酸化窒素吸入セッション、25%亜酸化窒素吸入セッション、プラセボ(50%窒素/50%酸素)吸入セッションを各セッション1時間、セッションの間隔1か月間で施行された。精神症状などの評価は、吸入前、吸入後22-28時間、1週間後、2週間後に施行。
・主要評価項目はHAM-D21
結果
・28名がエントリー。うち20名が3回の吸入を完了。4名が1回の吸入を完了。解析はこの24名を対象に行われた・参加者の平均罹病期間17.5年。エントリー時点でのHAM-D21得点の中央値は20.5点、MADRS中央値は30点
・吸入2週後のHAM-D21は50%笑気吸入後、25%笑気吸入後いずれもプラセボよりも有意に良好。50%と25%の差は有意ではなかった。プラセボとの有意差は両群ともに2時間後および24時間後では有意ではなく、2週目で明らかな有意差がみられた
3回のセッション全て完了した20名について、ベースラインのHAM-D21得点中央値は20.5点であったが試験完了時には8.5点へと、有意にうつ症状が改善した。試験終了時には、20名中11名(55%)が反応群(HAM-D21で50%以上改善)となり、20名中8名(40%)が寛解(HAM-D21で7点以下)となった・亜酸化窒素による抗うつ作用は少なくとも2-4週間は継続する可能性がある
・副作用については、50%笑気ガス吸入後には嘔気21%、頭痛17%、めまい13%、笑い13%、離人感 26%などで、25%笑気ガス吸入後では嘔気5%、頭痛10%などであり、有意に50%亜酸化窒素吸入後の方が副作用が多かった
コメント・2015年の結果と比較して、治療効果の速効性は再現されませんでしたが、25%亜酸化窒素、50%亜酸化窒素ともに治療抵抗性うつ病患者に対してプラセボより有意な治療効果を示しました。3か月間での全体でのHAM-D21得点変化量は11点であり、抗うつ薬の臨床試験を上回る数値となりました。
・問題点としては、二重盲検試験でしたが、亜酸化窒素の鎮静作用により亜酸化窒素吸入か、プラセボであるかは5人中4人以上の患者で判別可能であった点で、これによるunblinding biasは混入しうることです。
・副作用が強い薬剤では起こりうることですが、被検者がこれにより実薬かプラセボかわかってしまい、盲検性が確保できず、それによるバイアスが混入しうる問題があります。これについてはエスケタミンなどの臨床試験でも同様のことがいえ、さらに三環系抗うつ薬など、古い向精神薬における臨床試験でも、このunblinding biasが結果に影響を与えた可能性を指摘する報告もあります(Holper and Hengartner BMC Psychiatry (2020) 20:437)。unblinding biasが混入しプラセボがプラセボとわかってしまうと、プラセボ反応率は低下します。当然治療薬の効果量は増します。このところの新規抗精神病薬のプラセボ反応率が上昇してきているのは、新規抗精神病薬の安全性が向上し、unblinding biasが混入しにくくなっていることも一因としてありうるのかもしれません。
-
認知症とうつ
2021年06月29日
・メタ解析においては抜け落ちてしまう情報もあります。時にそれが本質的に重要な情報である場合もあります
・下の図は2018年の認知症+うつに対する抗うつ薬の有効性についてのメタ解析(Cochrane Database Syst Rev. 2018 Aug 31;8)ですが、これだけみると、ああ、抗うつ薬効かないのか、という結論になります。
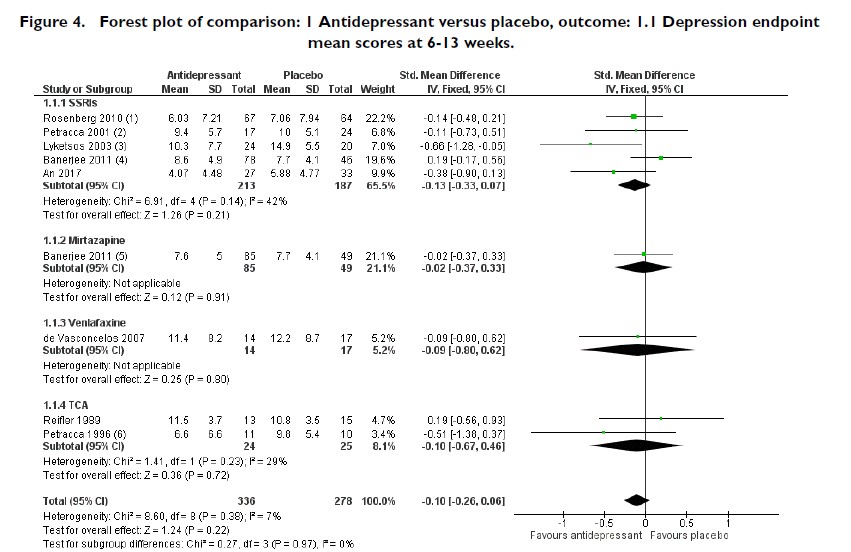
・しかし、元データをみると、より重要な情報が含まれていることがわかります。たとえばアルツハイマー型認知症のうつ症状に対するミルタザピンとセルトラリンのプラセボ対照比較試験(Lancet. 2011 Jul 30;378(9789):403-11 )でのCSDD(Cornell Scale for Depression in Dementia)の経時変化が以下です
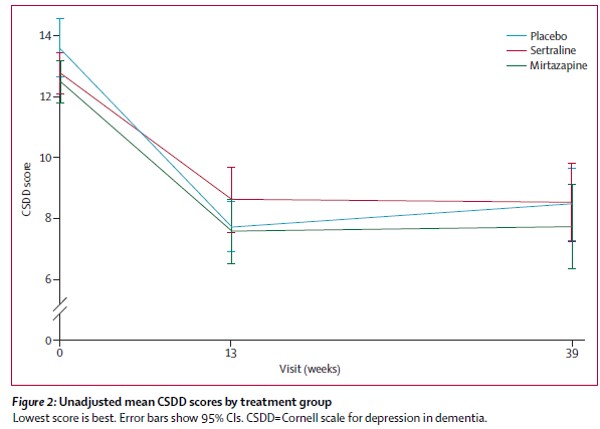
・さらに別のアルツハイマー型認知症のうつ症状に対するセルトラリンのプラセボ対照比較試験(Am J Geriatr Psychiatry. 2010 Feb;18(2):136-45 )のCDSSの経時変化は以下となります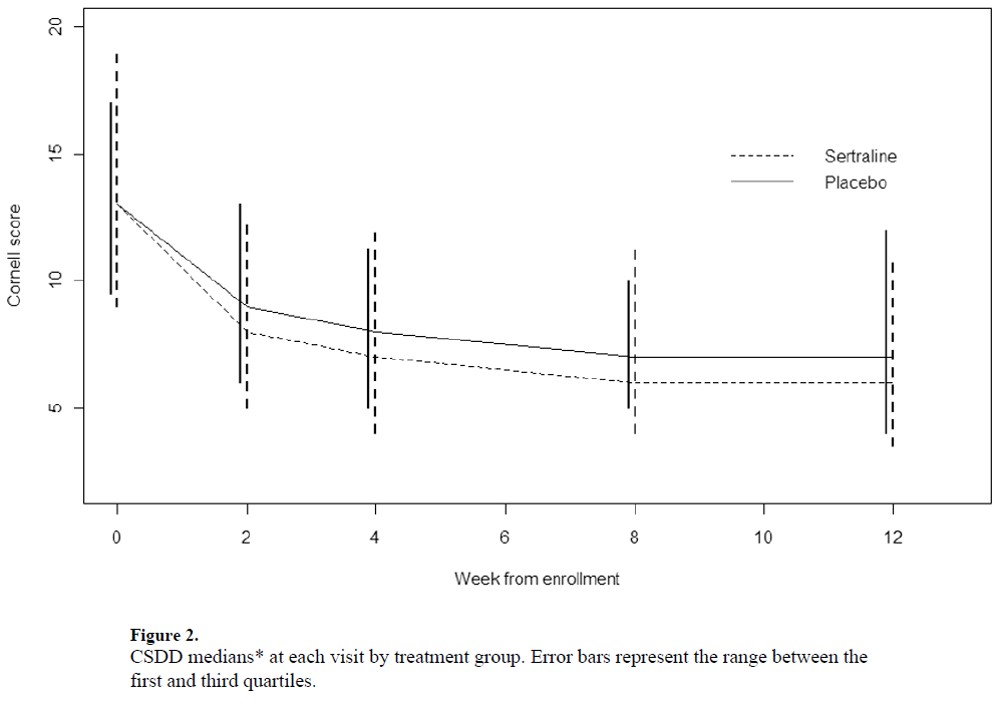
・これらのデータをみて、何がわかるでしょうか。それはプラセボが良く反応しているということです。そこから認知症のうつに対しては環境的介入が重要そう、ということが推測できます。このような情報はメタ解析からは読み取れません。・今回、このような観点から、環境的介入と薬物療法、通常ケアなどを比較したネットワークメタ解析の結果(文献1)が報告されたのでみてみます。結果として有効であると主張されている内容の一部にはネットワークメタ解析であるが故の脆弱なものも含まれており(わずかn=14の介入試験の結果が有効であると主張されているなど)、注意して解釈する必要があります。
・薬物療法による介入がぱっとしないことは予想できるのですが、いろんな手法の存在する非薬物療法的介入において、どれがよさそうか、についてはある程度知っておいてよさそうです。ただし薬物療法の場合の二重盲検試験と比較して、非薬物療法はよくてsingle blindなので、よりバイアスも入りやすく、質が異なるものを比較しているという点で注意が必要となります。
認知症とうつ(文献1)
背景
・認知症患者の約16%は大うつ病の診断を受け、32%は周辺症状として診断閾値下のうつ症状を経験している。
・認知症ではうつ症状は身体的症状(食欲不振、エネルギー低下など)や行動的症状(イライラ、社会的孤立、悲しみなど)として表出される
・認知症のうつ症状は、QOLの低下、機能低下、死亡リスクの増加などと関連し、介護者の苦痛、負担、抑うつの増加とも関連する
・認知症患者の大うつ病と抑うつの治療には、薬物療法(抗うつ薬、抗精神病薬など)および非薬物療法(回想法、運動療法など)が行われているが、抗うつ薬投与の有害性(転倒など)が報告され、非薬物療法の重要性が認識されている
・しかし、薬物と非薬物の効果を直接比較した無作為化試験はまれであり、エビデンスが乏しい。今回薬物療法と非薬物療法をネットワークメタ解析で比較した
方法と対象
・解析対象となったのは、認知症患者の周辺症状としてうつ症状を有する患者(非大うつ病)ないし認知症に大うつ病を合併する患者のうつ症状に対する薬物療法ないし非薬物療法についての無作為割付比較試験 N=235
・認知症周辺症状としてうつ症状を有する患者対象(非大うつ病)にした試験N=213
・認知症に大うつ病を合併する患者を対象にした試験 N=22
非薬物療法の介入内容としては以下のようなものに分類された(Nはnodeの数)
・通常ケア:患者のニーズと好みに基づいて、医療と社会的ケア(例:入浴などの日常生活動作のサポート)を適切に利用することと定義 N=102(非大うつ病)、N=6(大うつ病)
・アニマル・セラピー:動物と過ごすこと N=2(非大うつ病)
・経皮的電気刺激:経頭蓋的電気刺激 N=7(非大うつ病)
・回想法 N=26(非大うつ病)
・レクリエーション療法:ゲームや料理、読書など N=33(非大うつ病)
・リアリティー・オリエンテーション N=4(非大うつ病)
・心理療法:認知行動療法、カウンセリング、問題解決療法、力動的対人関係療法、支持的療法など N=24(非大うつ病)
・認知症患者へのサポート:当事者への電話や情報提供などによる心理社会的サポート N=1(非大うつ病)
・作業療法 N=15
・音楽療法 N=25
・多職種連携ケア:複数のヘルスケア専門家によるケアプランの作成 N=11(非大うつ病)、N=1(大うつ病)
・複数の感覚刺激:活動や物を通じて異なる感覚刺激を統合する N=5(非大うつ病)
・日常生活動作の修正 N=4(非大うつ病)
・マッサージとタッチセラピー:マッサージ、鍼治療など N=4(非大うつ病)、N=1(大うつ病)
・高照度光療法 N=4(非大うつ病)
・社会的交流:介護者やその他の人との交流 N=22(非大うつ病)
・運動:エアロビクス、バランストレーニング、レジスタンス運動など N=30(非大うつ病)、N=4(大うつ病)
・環境修正 N=3 (非大うつ病)
・介護者と当事者への教育 N=7(非大うつ病)
・介護者への教育 N=17(非大うつ病)、N=2(大うつ病)
・深部脳刺激 N=2(非大うつ病)
・認知リハビリテーション:治療目標を設定したリハビリテーション介入 N=27(非大うつ病)
・認知刺激療法:週に1-2回の認知機能賦活セッション(ゲームや芸術療法など) N=27(非大うつ病)
・介護者へのサポート N=3(非大うつ病)
・アロマテラピー N=2(非大うつ病)
非抗うつ薬系の薬物療法としては以下のnodeを設定
・抗菌薬:ドキシサイクリン+rifamin N=1(非大うつ病)
・降圧薬:nomidipine、プロプラノロール N=3(非大うつ病)
・抗精神病薬 N=21(非大うつ病)
・コリンエステラーゼ阻害薬 N=18(非大うつ病)
・dextromethorphan+キニジン N=1(非大うつ病)
・etanercept N=1(非大うつ病)
・ホルモン治療:エストロゲン、DDAVP、オキシトシン、プロゲステロン N=10(非大うつ病)
・高脂血症治療薬:アトルバスタチン N=1(非大うつ病)
・メマンチン N=6(非大うつ病)
・気分安定薬:カルバマゼピン、リチウム N=2(非大うつ病)
・プレドニゾロン N=1(非大うつ病)
・精神刺激剤:メチルフェニデート N=1(非大うつ病)
・鎮痛薬:アセトアミノフェン、オピオイド N=2(大うつ病)
抗うつ薬についてはN=15(非大うつ病)、N=18(大うつ病)
・評価尺度としては、Cornell Scale for Depression in Dementia(CSDD)がN=100、Geriatric Depression ScaleがN=58、Neuropsychiatric Inventory - DepressionがN=38など
・試験期間は11週未満がN=109(43%)、11-20週がN=78(30.5%)、21-30週がN=29(11%)、31週以上がN=40(16%)
・主要評価項目は、各試験使用されたうつ尺度の標準化平均差を求め、それをCSDD得点の平均変化量に変換したものを用いた
結果ネットワークメタ解析で有意差があった組み合わせは(かつnodeの試験の数が複数あるもの)以下の通り
。回想法は介護者支援より有意に良好 SMD 1.03
・回想法は認知リハビリテーションより有意に良好 SMD 0.42
・回想法は通常ケアより有意に良好 SMD 0.45
・認知刺激療法は回想法と有意差なし
・マッサージ+タッチセラピーは回想法より有意に良好 SMD 1.32
・認知刺激療法は介護者サポートより有意に良好 SMD 1.15
・認知刺激療法は認知リハビリテーションより有意に良好 SMD 0.53
・認知刺激療法は音楽療法より有意に良好 SMD 0.38
・認知刺激療法はプラセボと有意差なし
・認知刺激療法は心理療法と有意差なし
・認知刺激療法は通常ケアより有意に良好 SMD 0.57
・マッサージ+タッチセラピーは認知刺激療法より有意に良好 SMD 1.21
・マッサージ+タッチセラピーは作業療法より有意に良好 SMD 1.27
・作業療法は介護者サポートより有意に良好 SMD 1.07
・作業療法は通常ケアより有意に良好 SMD 0.51
・作業療法はプラセボとは有意差なし
・作業療法は介護者サポートより有意に良好 SMD 1.07
・作業療法は認知刺激療法と有意差なし
・多職種連携ケアは介護者サポートより有意に良好 SMD 0.96
・マッサージ+タッチセラピーは多職種連携ケアより有意に良好 SMD 1.38
・多職種連携ケアは通常ケアより有意に良好 SMD 0.39
・マッサージ+タッチセラピーはアニマルセラピーより有意に良好 SMD 1.32
・マッサージ+タッチセラピーは抗精神病薬より有意に良好 SMD 1.82
・マッサージ+タッチセラピーは高照度光療法より有意に良好 SMD 1.83
・マッサージ+タッチセラピーは抗うつ薬より有意に良好 SMD 1.76
・マッサージ+タッチセラピーは介護者教育より有意に良好 SMD 1.57
・マッサージ+タッチセラピーはコリンエステラーゼ阻害薬より有意に良好 SMD 1.52
・マッサージ+タッチセラピーは認知リハビリテーションより有意に良好 SMD 1.74
・マッサージ+タッチセラピーは運動より有意に良好 SMD 1.5
・マッサージ+タッチセラピーは多職種連携ケアより有意に良好 SMD 1.38
・マッサージ+タッチセラピーは音楽療法より有意に良好 SMD 1.58
・マッサージ+タッチセラピーは心理療法より有意に良好 SMD 1.55
・マッサージ+タッチセラピーは通常ケアより有意に良好 SMD 1.77
・Pairwiseのメタ解析結果で通常ケアと有意差があったのは運動療法 SMD 0.47
・非大うつ病患者において、ネットワークメタ解析で通常ケアと有意差があったのは、認知刺激療法 SMD 0.57、マッサージとタッチセラピー SMD 1.77、多職種連携ケア SMD 0.39、作業療法 SMD 0.51、回想法 SMD 0.45
・薬物による介入だけでは、通常のケアよりも有意に効果が高いものはなかった
・大うつ病患者においては、試験の異質性からネットワークメタ解析が施行できなかった。SSRI(sertraline、fluoxetine、citalopram、escitalopram)とプラセボの有効性を比較した7つのRCTについての結果は一定していない
・ミルタザピンおよびベンラファキシンもプラセボと比較してうつ病の症状の有意な改善とは関連していなかった
・1つの無作為化比較試験において、多職種連携ケアは通常の治療よりも効果的であることが報告されたが、他の非薬物介入(心理療法と運動)の効果を支持するエビデンスは不十分である
コメント・マッサージ+タッチセラピーについてはかなり高い効果量が出ていて違和感があるのですが、2つのグループから対通常ケアでの3つの介入試験(n=219)が報告されています。この3つの試験のRisk of Biasについては評価者のblindingおよびmissing dataの扱いいずれもlowとなっており、試験の質はそこまで低いとは言えないようです。ただ有効性についての結果が目立ちすぎているのは気になります。
・なお論文中で通常ケアと比較して有効とされた認知刺激療法+コリンエステラーゼ阻害剤、社会的交流+認知刺激療法+運動については、それぞれ1つの介入試験しかなく(特に後者はn=14のみ)、エビデンスの質としては低いため、結果からは除外しています
引用文献
文献1:Jennifer A Watt et al. BMJ 2021;372:n532 | doi: 10.1136/bmj.n532
-
Prof. Stefan Leuchtとのやりとり
2021年06月20日
・もともとはBMJで認知症のうつについてのネットワークメタ解析の論文(BMJ 2021;372:n532 | doi: 10.1136/bmj.n532)が出たので、それについて記事にしようかと思ったら、思いがけない方向にいってしまったので、まとめておきます。
・そもそもネットワークメタ解析については、いろんな批判もあり、以前も触れたようにバイアスの影響をとても受けやすいこと(Trinquart L et al. PLoS One. 2012;7(4):e35219. doi: 10.137)や、組み込まれた各試験のエビデンスの質がわかりにくく(この点、従来の直接比較のメタ解析のforest plotは、何本の介入試験が統合されているのかなどの情報が明示されるため、まだ直感的にわかりやすい)、結果の解釈には注意を要します。
・その点において、2020年の藤田医大の岸先生らの報告(Kishi T et al. Mol Psychiatry. 2020 Nov 11. doi: 10.1038/s41380-020-00946-6)にみられたようなConfidence in Network Meta-Analysis (CINeMA)を用いたgrade表記などは、ネットワークメタ解析における結果の信頼性を併記するという点で素晴らしいものだと思いました。
・ネットワークメタ解析の結果に注意すべき具体例を挙げると、例えば2011年のBMJ誌に掲載された全般不安症に対するネットワークメタ解析の論文(BMJ. 2011 Mar 11;342:d1199. doi: 10.1136/bmj.d1199.)があります。
・結果を見ると、やたらフルオキセチンの結果が良好で、有効性に関して第一位、フルオキセチンすばらしいという結論になっているのですが、いざその根拠となった論文をみてみると、フルオキセチンについてはたった1つだけの介入試験しかなく、しかもフルオキセチンの症例数は33例、さらにこの介入試験は大うつ病に全般不安症を合併した症例に対するベンラファキシンとの比較試験です(純粋に全般不安症の患者を対象としたものではない)。
・従来のメタ解析においては、このような単一の介入試験がメタ解析の対象として組み込まれることはないので、まずこのようなバイアスリスクの高い結果を主張するようなことは起こりません。この報告をみて一気にネットワークメタ解析への信頼感が薄れ、警戒心が高まりました。少なくともこの報告については、科学的に信頼に足る結果とはとてもいえません。しかも著明な雑誌にこのような結果が掲載されてしまうのですから、恐ろしいことです。ネットワークメタ解析の結果については批判的に吟味しなくてはならないのはこのような理由からです。
・ちなみに現段階でそこそこあてにすべき全般不安症のネットワークメタ解析の結果は、2019年のlancet(Slee A. et al. Lancet. 2019 Feb 23;393(10173):768-777)あたりでしょうか。2020年にもより解析対象を絞ったネットワークメタ解析(Kong W. et al. Front Pharmacol. 2020 Nov 11;11:580858.)が出ていますので、こちらもチェックしておきたいところです。
・そのような実例を勉強会で具体的な例で示そうと思い、ちょうど良いと思って、統合失調症のpredominant negative symptom症例に対する介入試験のメタ解析の報告(Mark Krause et al. Eur Arch Psychiatry Clin Neurosci. 2018 Oct;268(7):625-639.)を基に、いかに従来型のメタ解析とネットワークメタ解析が異なり注意が必要かについて示そうと思ったら、思いがけず、元論文の間違いではないかという点を見つけてしまい(結果的に間違いとは言えなかったのですが)、corresponding authorのLeucht教授(世界的に超有名な方です)にメールしたところ、思いがけず返信をいただいて、その内容に納得したところです。
・まず、この論文の主要な結果を示します。
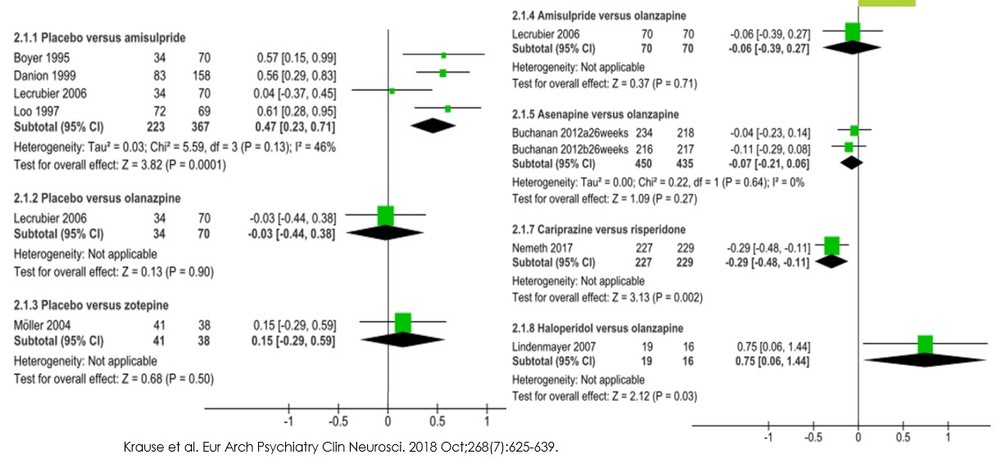
・この図でわかるように、メタ解析が可能なのはアミスルプリドくらいしかなく、他の薬剤については介入試験が1つか2つ程度しかないため、エビデンスは不十分であり、明確な結論を引き出すことができないことがわかります。直接比較のメタ解析では、このようなこともforest plotから読み取れるのでわかりやすいです。
・ところが、実際のところ、このようなデータしかなくても強引にネットワークメタ解析を施行することはできてしまいます。この点については、この論文の著者もネットワークメタ解析を当初行おうと思ったけども、結果のinconsistencyが大きく断念したと記載されています
・いざネットワークメタ解析をしようと思った場合、特にmulti-armsの介入試験の場合には元データから新たにデータを作り直す必要がある場合があるため、multi-armsの介入試験(この図ではLecrubier 2006にあたる)については元論文をあたって、元データを取り出して、そこからRでのネットワークメタ解析に使用できるデータに変換する必要があります。
・そこで元論文(Acta Psychiatr Scand 2006: 114: 319–327)を眺めてみたところ、主要評価項目はSANS summary scoreとなっています。結果はどうかというと、24週間でのベースラインからの変化量は、アミスルプリド群 -4.3点(SD 4.9)、オランザピン20mg群 -4.0点(SD 5.1)、オランザピン 5mg群-4.7点(SD 5.3)、プラセボ群 -3.1点(SD 4.8)とのことでした。ここから標準化平均差(SMD)を出すことは各群のnがわかれば手計算で簡単にできて、アミスルプリド群は0.237(SE 0.21)、オランザピン群は5mgと20mgをひとまとめにして、0.178(SE 0.209)となります、アミスルプリド群とオランザピン群とのSMDは-0.06(SE 0.169)となります。
・さて、Krauseらの論文とおんなじかなと思い確認したら、なんとこの論文ではアミスルプリドのSMD 0.04、オランザピンのSMD -0.03とあるではありませんか。この理由がどうしてもわからなくて、だめもとでLeucht教授にメールしてみました。そしたら思いがけず返信をいただいて驚愕しました。

・何度かやりとりをしたのですが、結論から言うと、Krauseらの論文では、主要評価項目としてPANSS negativeをまず第1に設定していて、その次にSANSなどとしており、どちらのデータもある場合にはPANSS negativeをとるということでした(Lecrubierらの論文の本文中にはPANSS negativeの数値がないのですが、おそらくどこからかデータをもってこられたのでしょう)。あらかじめ設定したルールに従って解析したということです。
・ただ陰性症状の評価尺度としてはSANSの方が優れているので、この点は確かに議論の対象となりうることだとメールにありました。Leucht教授は精神医学の分野におけるEBMにおいては世界トップクラスの業績を上げておられ、極めて重要な論文も数多く公表されおられる大先生で、お忙しい中このような日本の片田舎の一臨床医の質問にも丁寧にお答えいただき実にありがたいことでした。
・というわけで私は、SANSを使って勝手にネットワークメタ解析を進めたわけですが、その結果は以下となります。(いつものようにRのnetmetaパッケージを使って、頻度論によるネットワークメタ解析をしています)
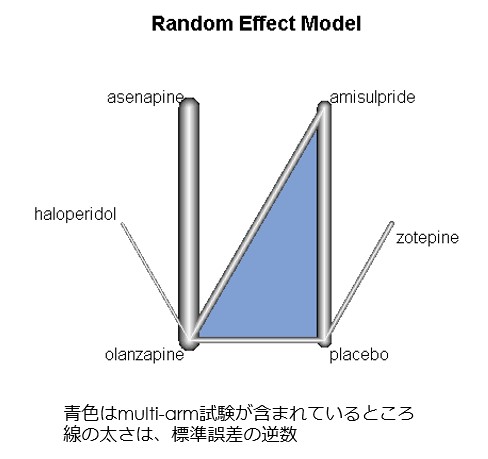
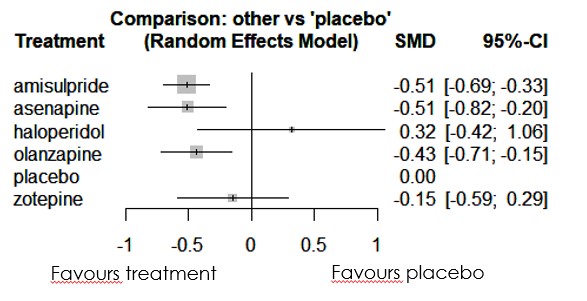

・このような解析をしてはいけませんよという注意喚起でやってみたネットワークメタ解析ですが、なにやら面白そうな結果がでてしまいました。Meiji SeikaファルマのMRさんが喜ぶかもしれない結果ですが、この結果も先に述べたようにエビデンスの質という観点から注意して解釈いただくことが必要となります(規模はまあまあ大きく、異質性も小さいのですが、アセナピンについては1つのグループだけからの2つの介入試験の結果から構成された結果のため)。
・ちなみにKrauseらのデータによるNMAでは問題となったinconsistencyの問題ですが、Lecrubierらの論文に関してSANSを使用すると、inconsistencyは問題なく、異質性に関する指標I^2についてもQ^het=0.343, d.f.=3から0となり(ネットワークメタ解析では、I^2=max((Q-d.f.)/Q,0)で決定するため)問題がない状況に落ち着いています。
・この結果にpartial agonistがどう食い込んでくるのかなど、今後注目すべき事柄となります。




