ピマバンセリン
2021年12月09日
・ピマバンセリンと言えば、セロトニン2A受容体の逆作動薬であり、パーキンソン病に伴う幻覚妄想症状に対してFDAの承認を得ていることで知られていますが、今年7月にはNEJM誌に認知症全般における精神病症状について、再燃予防効果を検証するプラセボ対照試験が報告されました(N Engl J Med. 2021 Jul 22;385(4):309-319)
・この報告では、オープン試験期間中にピマバンセリンの有効性がみられた(投与開始8週時点および12週時点でSAPS-H+D総得点でベースラインと比較して30%以上の改善+CGI-Iで1点か2点を満たすもの)ケースについて、プラセボに置換した場合と継続投与された場合との二重盲検無作為割付比較試験が行われました。その結果、再発率は26週間で、ピマバンセリン群で13%、プラセボ群で28%(再発までの期間のハザード比、0.35;95% CI 0.17~0.73;P=0.005)となり、再発リスクを65%低下させたというものでした。ただし認知症のサブタイプについて解析すると、その有効性についてプラセボとの有意差がみられたのはパーキンソン病認知症のみであり、アルツハイマー型認知症に限って解析すると、再発リスクについてプラセボとの有意差はみられなかったというものでした。
・今回は、統合失調症のpredominant negative symptomに対するピマバンセリン上乗せの有効性に関するプラセボ対照試験が報告されました(Bugarski-Kirola D et al. Lancet Psychiatry. 2021 Nov 30:S2215-0366(21)00386-2. doi: 10.1016/S2215-0366(21)00386-2. Online ahead of print. )。
・predominant negative symptomは主として慢性期における一次性陰性症状が主体で陽性症状が目立たない状態のことでprominent negative symptomは陰性症状を強く認めるものの、陽性症状も混在する状態として定義されているようです。ここで一次性陰性症状と二次性陰性症状とは、以下の図で示す通りの概念となります(竹内 啓善 臨床精神薬理 12:2083-2102、2009より引用)
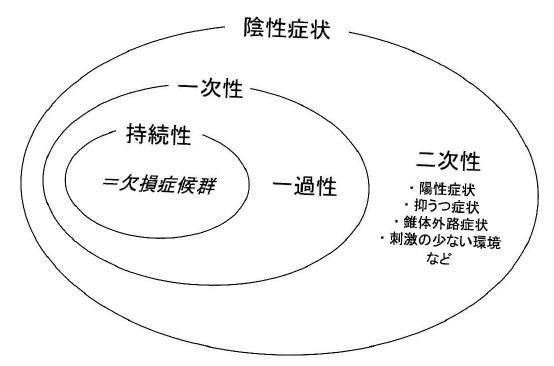
・一次性陰性症状の中核に位置する欠損症候群の診断基準には、感情の狭小化、情動変化の減少、会話の貧困化、興味の減少、目的意識の低下、社会性の低下の6つの項目が含まれており、その診断の詳細については上記竹内先生の文献を参照ください。二次性陰性症状には抑うつなども含まれるため、いかに純粋に一次性陰性症状を抽出するかがポイントになります。そのためにSANSなどの評価尺度が用いられているのですが、今回のBugarskiらの報告ではNSA-16という尺度が用いられました。ちなみに陰性症状にはPANSS negativeもありますが、PANSS negativeは一次性陰性症状の評価には不適切といわれており、その理由としてPANSS negativeに含まれる抽象的思考の困難や常同的思考については、陽性症状主体であっても得点が高くなりうることがあげられます。そのため例えばpredominant negative symptomに関して、カリプラジンがリスペリドンよりも優れていることを示した2017年のLancet論文(Nemeth G et al. Lancet. 2017 Mar 18;389(10074):1103-1113)では主要評価項目にPANSS-factor score for negative symptom(PANSS FSNS:N1、N2、N3、N4、N6、G7、G16の合計点)が使用されています。
・今回の報告で用いられたNSA-16 については並木らの解説(並木千尋ら 精神医学 58:469-480. 2016 )があり、引用させていただくと、下図のような項目から構成されている評価尺度となります。

Predominant negative symptomに対するピマバンセリン
背景
・統合失調症の陰性症状や認知機能障害は、統合失調症の疾病負荷の大きさを陽性症状よりもよく予測しうるといわれている。しかしその治療法はない
・D2遮断は健常者でも陰性症状類似の症状を惹起するといわれている。一方でセロトニン2A遮断はNMDA受容体アンタゴニストに起因する症状を緩和し、線条体と大脳新皮質のドパミン放出を増加させるといわれており、陰性症状にも効果があるのではないかといわれている。
・いくつかの非定型抗精神病薬はおそらくはセロトニン2受容体への親和性がD2受容体への親和性を上回るために、二次性陰性症状に対する効果があるといわれている。しかし一次性陰性症状に対する非定型抗精神病薬の有効性はよくわかっていない
・例えば、アミスルプリドとジプラシドンは陰性症状を改善することが報告されているが、これは二次性陰性症状の改善に起因するものかもしれない
・カリプラジンはリスペリドンに対して陰性症状主体の統合失調症患者において有意に良好な結果を示したが、プラセボが含まれていない問題があり、さらに検証を要する。
・2018年のメタ解析では抗うつ薬増強が陰性症状に有効である可能性が示された(第1世代への増強の場合のみ)が、すべての試験でベースラインのうつ症状の重症度が評価されたわけではないため、うつ症状に対する効果が交絡し、二次性陰性症状に対する効果をみている可能性がある
・これまでにセロトニン2Aアンタゴニストや逆作動薬であるM100907、volinanserin、eplivanserinなどで、陰性症状に対する効果についての予備的な結果が報告されている
・選択的セロトニン2A/2C受容体拮抗薬であるリタンセリンは、プラセボ対照試験で陰性症状に対する有効性を示唆する結果が報告されている。
・ピマバンセリンはセロトニン2A受容体逆作動薬であり、そのほかの受容体への親和性がほとんどない。FDAはパーキンソン病の幻覚妄想に対してピマバンセリンを承認している
・第2世代抗精神病薬治療により安定している陰性症状主体の統合失調症患者に、ピマバンセリンを上乗せすることにより、大脳新皮質のドパミン放出が増加し、陰性症状に対して効果が期待できるのではないかとの仮説のもとで、プラセボ対照試験を実施した
対象と方法
・18-55歳の外来統合失調症患者(DSM-5)。SCID-CTで確認されたもの。平均罹病期間11.8年
・罹病期間1年以上で、最近12週間以上安定しているもの
・PANSS Marder negative factor itemsで20点以上(7項目中3項目以上で4点以上もしくは7項目中2項目以上で5点以上)かつPANSS Mader positive factor items8項目の合計が22点以下(4点が2項目以下である、かつ5点以上がないこと)
・CGI-SCH-S(Clincal Global Impression of Schizophrenia Scale-Severity)の陰性症状尺度が4点以上(中等症以上)。CDSS9点以上のうつ症状を有する者は除外。
・十分量のアリピプラゾール、アリピプラゾールLAI、アセナピン、ブレクスピプラゾール、カリプラジン、ルラシドン、オランザピン、リスペリドン、リスペリドンLAIによる8週間以上の治療を受けており、血中濃度で確認された治療アドヒアランスが良好であること。定型薬は不可
・試験期間:スクリーニング4週間、盲検期間26週間、フォローアップ4週間
・非定型抗精神病薬+ピマバンセリン 10から34mg n=201 (10mg 3%、20mg 45%、34mg 54%)
・非定型抗精神病薬+プラセボ n=202
・主要評価項目:26週間のNSA-16の変化量
・副次評価項目:Personal and Social Performance scale (PSP)、 PANSS total、CGI-SCH-I(1点ないし2点を反応群と定義)、BACS、DAI-10など
結果
・併用薬剤はアリピプラゾールないしアリピプラゾールLAIが約33%、リスペリドンないしリスペリドンLAIが約39%、オランザピンが約28%、ルラシドンが1%
・26週間でのNSA-16得点の変化量はピマバンセリン群で有意に良好(最小二乗平均差 -1.9点。Cohen’s d=0.211)
・副次評価項目では有意差なし(NSA-16の20%以上改善の反応率 53%対49%、CGI-SCH-I反応率 32%対29%、PSP得点の変化量有意差なしなど)
・多い有害事象は頭痛(プラセボ群5%、ピマバンセリン群 6%)、傾眠(プラセボ群 5%、ピマバンセリン群 5%)。副作用による中断率はプラセボ群3%、ピマバンセリン群 5%
議論
・事後解析では34mg投与群はより低用量投与群より陰性症状改善度が良好であることを示唆する結果がえられており、全体の54%しか34mgを投与されなかったことを考慮すると、高用量ではさらに良好な結果がえられた可能性はある。しかしPETでの試験ではピマバンセリン20mgでセロトニン2A受容体はほぼ完全に占有されることから、34mgでの効果は、さらに別のセロトニン2Cなどの影響が寄与しているかもしれない。
コメント
・効果量は小さく、有意差がでたとはいえ、それほど大きな臨床的有効性は期待できない結果となりました。ただし、併用した薬剤毎の解析結果はどうなのでしょうか。アリピプラゾールはセロトニン2A遮断は強くないですし、ピマバンセリン併用でより高い効果が期待できそうな気もします。またリスペリドン群ではリスペリドンの用量が気になるところです。ピマバンセリンはリスペリドンよりもセロトニン2A受容体に対する親和性が高いとはいえ、同じセロトニン2A逆作動薬であるリスペリドンの併用下では、ピマバンセリンの作用は目立たなくなるのではないかと思われるためです(それでもリスペリドン2mgへの併用では効果がみられたとの報告もありますが:Herbert Y. Meltzer et al. Schizophrenia Research 141 (2012) 144–152)




