-
治療反応性予測はどこまで可能か
2022年07月25日
・fMRIなどを用いて、抗うつ薬による治療反応性を予測しようというEMBARC試験の結果が報告されました(文献1)。結果は寛解に関して予測モデルのc-indexは0.6台と高くはないようですし、画像所見だけでは予測モデルの構築には不十分で、様々な臨床的特徴も組合わせることにより予測精度が上がっているようですが、今後の進展が期待される領域といえそうです。
報酬タスクによる治療反応性予測
背景
・抗うつ薬の治療反応性に関するバイオマーカーの発見は重要である。現在、個々の抗うつ薬の寛解率は通常40%以下であり(Dupuy et al. The international journal of neuropsychopharmacology 14: 1417–1431.)、約33%が寛解に至るまでに3~4回の薬物試験を必要とする(STARDの結果より。Rush et al. American Journal of Psychiatry 163: 1905–1917)。
・治療を最適化するバイオマーカーや予測ツールがあれば、寛解を早め、個別化医療を実現することができる
・安静時fMRIにおけるデフォルトモードネットワークと海馬の結合は、セルトラリンの治療成績と相関することが報告されている(Chin et al. American Journal of Psychiatry 177: 143-154. 2019)
・ネガティブな感情を誘発する写真提示時における前部帯状回の活性化が大きいことが、ベンラファキシンに対する治療反応性が良好であることと関連することが報告されている(Davidson et al. American Journal of Psychiatry 160: 64–75. 2003)
・様々な表情画像を提示した際の扁桃体の活性化が大きいと、その後の症状改善度が良好であることと関連することが報告されている(Canii et al. Neuroreport 16: 1267–1270.2005
・今回、治療開始前の報酬課題におけるfMRIの測定結果と治療効果の間の複雑で非線形な関連性を発見するのに適した深層学習モデルを採用し、最も情報量の多い特徴量を抽出することで、治療反応性予測モデルを構築し、その予測精度を評価した
対象と方法
・うつ病患者296名。30歳以前の発症で、慢性経過(エピソード期間2年以上)または再発性の経過(エピソード2回以上)の患者
・第1ステージでは、セルトラリンまたはプラセボ群に無作為に割付され。 8週目に奏効基準(CGIで「大幅に改善」未満)を満たさないセルトラリン群は、第2ステージのブプロピオン投与群にクロスオーバーされさらに8週間二重盲検で追跡
・主要評価項目:HAM-D改善度
・ベースラインおよび報酬課題中にfMRIを施行。
・報酬課題では被検者は画面に提示される数字が、5よりも大きいか、小さいかを予測する課題を行う。被検者がそのどちらかの選択肢を提示し、その後画面に“おそらく勝ち(possible win)”もしくは“おそらく負け(possible loss)”の2種類のカードが提示される。その後正解が提示され、“おそらく勝ち”を提示されて実際の数字が当たりであったら1ドルの報酬を得て、“おそらく勝ち”を提示されて負けた場合には罰は与えられない。一方で“おそらく負け”を提示され、実際に外れていたら0.5ドルを失い(罰)、一方で“おそらく負け”を提示されて実際の数字があたりであったら罰はないが報酬もない。
・fMRIにより罰する試行と報酬を与える試行の間の活性化の差(報酬期待:reward ecpectancy)、各推測試行の初期予期段階、予測誤差(誤判定後の差: prediction error)の3種類の脳活動を定量化。各被験者200か所の脳機能領域に分割。
・ベースライン特性として、家族歴、人種、民族、年齢、学歴、性別、配偶者の有無、HAM-D、MASQ、QIDS-SR16(治療前のうつ病重症度)、CTQ(小児期のトラウマ)、ASRM(躁症状)、CSSRS(自殺リスク)、STAI(不安)、エピソード期間、SAPAS(性格特性)などを評価。
・ベースライン特性、fMRI結果などを用いて深層学習を用いて治療反応性予測モデルを構築
結果
・セルトラリン投与群(n=106)における第1ステージでのHAM-D変化量は7.89、寛解率39%、反応率54%。セルトラリンの予測モデルは、HAM-D変化量の予測において、決定係数R2 48%、RMSE(Root Mean Squared Error) 5.15という良好な数値であった。
・セルトラリンの転帰を予測しうる主要な20の特徴のうち、半数は臨床的特徴であった。Psychomotor agitationと治療前の症状重症度(HAM-D得点)が高いほど、より大きな改善を予測した。自殺の家族歴,合併症(SCQ: Self-Administered Comorbidity Questionnaireの総得点),および最初の気分障害またはうつ病エピソードの年齢が高いほど,改善が少ないことが予測された
・セルトラリン投与群の治療反応性とfMRI所見との関連については、報酬期待時における右下前頭回三角部での高い活性化、初期予期段階での右中後頭回と右中側頭回での高い活性化、prediction error時における右上側頭回での高い活性化などが治療反応性が良好であることと関連した。
・改善度が低いことは、prediction error時の左小脳left crus 1の活性化が高いこと、報酬期待時に右縁上回と右後部帯状回で活性化が高いこと、初期予期段階で左上前頭回の活性化が高いことなどから予測された
・プラセボ群(n=116)では、第1ステージにおける平均HAM-D変化量は6.70で、セルトラリン群と有意差なし。寛解率は33%、反応率は35%。
・アジア系人種、別居の配偶者があること(わずか3名のみのため真の相関ではない可能性あり)、NEOでのopenness得点、気分不快のない期間の長さなどがプラセボ反応率が良好であることと相関した。一方でパニック症、過眠症の合併、高齢、アンヘドニアの存在はプラセボ反応率が不良であることを予測した
・fMRIの結果とプラセボ反応率との関連については、プラセボ反応率が高いことは、初期予期段階で右中後頭回の活性化が高いこと、報酬期待時における右縁上回の活性化が高いこと、prediction error時の左上側頭回、右下後頭回、左上頭頂小葉の活性化が高いことによって予測された。
・プラセボ反応率の低さは、prediction error時の左小脳、右中側頭回、左中前頭回で活性化が高いこと、初期予期段階で左下後頭回の活性化が高いことなどから予測された。
議論
・すべての治療群において、前頭葉領域の活性化は、HAM-Dの改善度が小さいことを予測した。 興味深いことに、小脳領域の活性化はすべてのモデルで治療反応性の予測と関連した。小脳は伝統的に運動制御と関連しているが、最近では、小脳は報酬処理との関連が報告されている。例えば、報酬処理中の小脳crus 1と前頭前野間の機能的結合は、うつ病で上昇することが報告されている(Tepfer et al. . Depress. Anxiety 38: 508–520. 2021)。今回、prediction error時および報酬期待時の小脳活性化が、すべてのモデルで重要な予測因子であることが示された。これらの結果は、小脳、特にcrus1が今後の治療モデレータ研究のターゲットになりうることを示唆している
・海馬における報酬期待時の高い活性化は、より大きなHAM-Dの改善を予測した。海馬は、MRIによる体積測定とPETによる代謝活動により、うつ病の気分調節障害に関与していることが示唆されている
コメント
・残念ながらfMRI所見だけからでは、治療反応性の予測精度はc-index 0.5台と低く、様々な臨床的特性を組み合わせる必要があるようです。今後さらに大規模データの蓄積により、予測精度が向上することが期待されます。ちょうど慶應の野田先生、中島先生らのMultidisciplinary Translational Research LabのrTMS研究でも治療反応性予測にも関連した研究をされているとのことで、薬物療法で least predicted improvementとされた群に関して、rTMSなどを効果的に適応できるような方向性がみいだせるとprecision medicineにもつながりうることで今後の進展に期待したいと思います。
文献1:Kevin P Nguyen et al. Biol Psychiatry. 2022 Mar 15;91(6):550-560. doi: 10.1016/j.biopsych.2021.09.011. Epub 2021 Sep 22. -
rapid cycling
2022年07月10日
・ラピッドサイクリングについてのメタ解析が出たので(文献1)、感想を述べたいと思います。
・まず最初に、解析に使用されているwithin subjects meta-analysisというのが、非常に一般的ではありません。
・通常のメタ解析ではプラセボなどの対照薬との比較をして、効果量を出してそれを統合したりしますが、この報告では、治療前後のアウトカム(MADRSやYMRSなど)の変化量を効果量に換算し、統合しています。さらにそれをプラセボ群についても同じこと(治療前後のアウトカムの変化量を効果量に換算して統合する)をして、そのプラセボ群の効果量の95%信頼区間と重なるかどうかで、対象とする薬剤が有意に効果があるかどうかを判断するという、かなりトリッキーなことをしています。このようにすることで、プラセボ対照ではない試験における対象薬の効果量も統合できるのはいいのですが、あまり一般化できそうにない結論がabstractに出てきてしまっています(本文では割と慎重な記載がされているのに、なぜかabstractではそのニュアンスが消えている)
・例えば、うつ病相においてベンラファキシンやシタロプラムの名前があったり(ベンラファキシンは双極II型のみを対象とした試験の結果に基づくので一般化はできないと思われますし、STEP-BDの知見からは抗うつ薬は病相回数を増やしてしまい、不安定化につながるのでよろしくないだろうとの結論であったはずです)、一方でクエチアピンの名前がなかったりなどです。
・クエチアピンは後程触れますが、rapid cyclingの急性期うつ病相において4つのプラセボ対照試験の事後解析結果などが報告されており、これらを通常のメタ解析で統合するとある程度しっかりとした有意な効果量が導けます。このようなメッセージをせめてsensitivity analysisなどで検証して、表に出してほしかったのですが、それがないのは残念でした。
Rapid cyclingにおけるwithin-subjects meta-analyses
背景
・Rapid cyclingでは、非RCと比べて、躁病エピソードが約7倍、うつ病エピソードが約2倍と、エピソードの頻度が高いといわれている(Kupka et al. Am J Psychiatry. 2005;162(7):1273-1280. )。・Rapid cyclingの生涯有病率は双極性障害患者全体の26-43%であり、様々な身体疾患のリスクが高く、混合状態、物質使用障害、自殺傾向、より悪い心理社会的機能などの疾病負担の増大を伴うとされている。 治療ガイドラインでは、rapid cyclingに対する特定の治療法は推奨されていない
今回より多くの介入技法を含めてWithin-subjects meta-analysesをしてみた対象と方法
・無作為割付比較試験、クロスオーバー試験を含む
・10名以上の対象者が無作為化されたもの
・18歳以上の双極性障害患者でrapid cyclingの診断を満たすもの
・対照群としてプラセボ、他の薬剤、非薬物療法的介入、waiting list, treatment as usualを含む
・主要評価項目は、介入前後に評価された以下の連続尺度、1)CGIなどの包括的尺度、2)うつ症状評価尺度(MADRSないしHAM-D)、3)躁病症状評価尺度(YMRS)、4)改善(反応)までの時間や悪化までの時間を示すその他の評価項目
・治療前と治療後の各指標(MADRS、YMRS、CGIなど)を用いて、Within-subjectでの効果量Hedge’sg(治療前からどの程度改善したか)を導出した
これらをrandom effects modelで統合し、各治療群毎の効果量を算出・プラセボの効果量については、すべての試験の結果(異質性の高い一部試験は除外)の効果量を統合し算出
・ベースラインでうつ状態の患者を対象とした試験のみがうつ状態の結果の解析に、躁状態の患者を対象とした試験のみが躁状態の結果の解析に用いられた
Within-subject meta-analysesでは、群間比較での統計的有意差の有無は求めることができないため、各群の95%信頼区間が重複しない場合に、有意差ありと推定した結果
・30の試験結果を記述した34本の文献が解析対象となった
・介入期間は3週間から100週間までで、中央値は14週間。1 studiyはクロスオーバー試験で、1件のみ非薬物療法的介入(Cognitive psychoeducational therapy)の有効性を検討
・6 studies(20%)がバイアスリスク高と判定
・2 studiesでは、生涯平均で年間4回以上のエピソード、1 studyでは、平均月1回以上のエピソード、1 studyでは、2年以内に8回以上のエピソードであることが条件とされた。5 studiesでは、最大閾値を設定し、前年度にそれぞれ8、12、20回以上のエピソードがあった参加者を除外していた。16 studiesでは、BD の異なるサブタイプの参加者を募集し、9 studiesが 双極I型障害 のみ、5 studiesが 双極II型障害 のみを対象としていた。
(1)非定型抗精神病薬
・Global impressionでは、クエチアピンのwithin-subject効果量(治療前後のCGIの変化量から求めた効果量)は0.79で、抗精神病薬全体でも0.79であった。
・うつ症状については抗精神病薬全体(10試験)のうつ症状改善度の効果量は0.75であり、異質性が大きかった(69%)。 クエチアピンの効果量は非定型抗精神病薬全体と同等であった(0.76、37%の異質性)。うつ病のアウトカムで1試験以上実施された他の抗精神病薬はオランザピン(フルオキセチン併用ないし非併用含む)で、効果量は1.01であった(異質性0%)
・躁症状については、2つ以上の試験で検討された薬剤はなく、全体の効果量は1.11
(注)
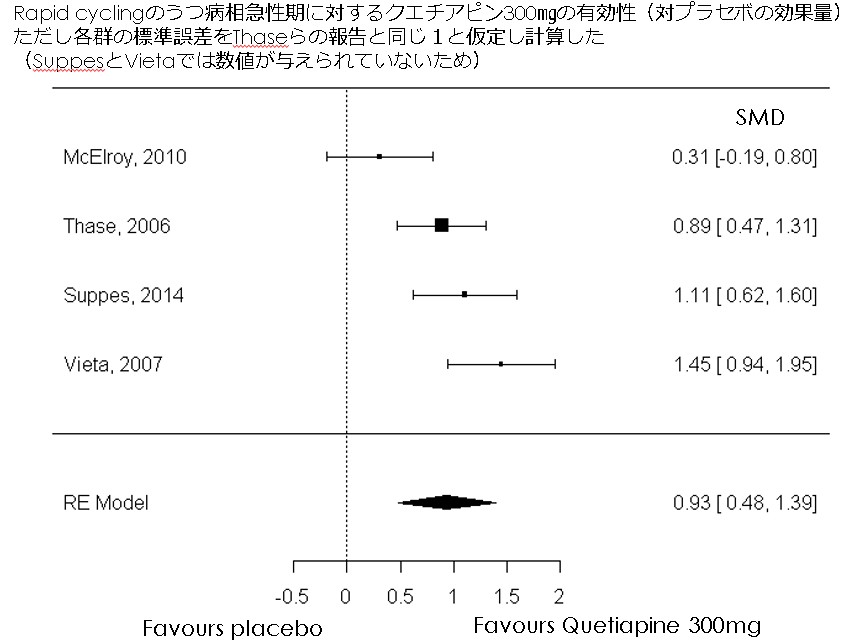
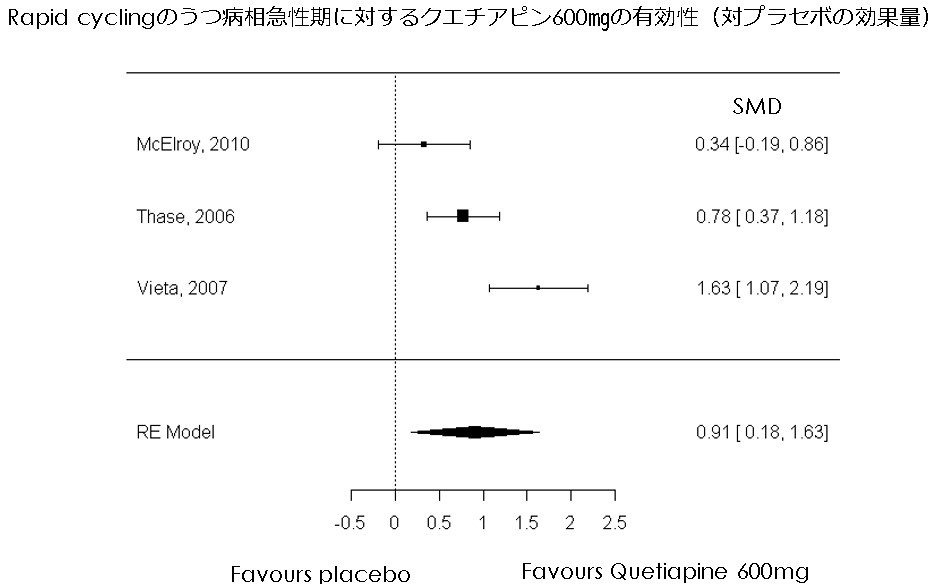
・Rapid cyclingのうつ病相急性期におけるクエチアピンのプラセボ対照RCTは事後解析も含めて以下の4つがあり、よりエビデンスの質が高いと思われる通常のpairwise meta-analysisが可能である(ただし、SuppesらとVietaらは標準誤差が与えられていないため、Thaseらの数値で代用しています。より厳密には標準偏差が同じと仮定してサンプルサイズの平方根で比率をとって標準誤差をだせばよいですが300mg群のサンプルサイズがそこまで違わないのでしてません)。通常のメタ解析を行うと、クエチアピン300mgもクエチアピン600mgもラピッドサイクリングの急性期うつ病相において有意に有効との結論がでる
・McElroyら 2010(EMBOLDEN II) 8 weeks MADRS変化量 Quetiapine 300mg -16.29(n=46), Quetiapine 600mg -16.08(n=35),プラセボ -14.37(n=24) 有意差なし SE 0.6?
・Thaseら 2006(BOLDER II) 8 weeks MADRS変化量 Quetiapine 300mg -19.99(n=44), Quetiapine 600mg -19.24(n=46), プラセボ -13.73(n=53) 有意差あり SE 1.0?
・Suppesら 2014 8 weeks MADRS変化量 Quetiapine 300mg -20.3(n=36),プラセボ -13.5(n=38) 有意差あり
・Vietaら 2007(BOLDER) 8 weeks MADRS変化量 Quetiapine 300mg -20.7(n=42), Quetiapine 600mg -21.1(n=31),プラセボ -11.6(n=35) 有意差あり
(2)気分安定薬
・ラピッドサイクリングに関して1つ以上の試験で検討されたのはリチウムとラモトリギンのみ
・Global Impression:5つの試験でプールされた効果量は0.67(異質性59%)。このうち3試験で検討されたラモトリギンは効果量が低かった(0.58、異質性61%)。
・うつ症状:リチウムは効果量が比較的高く(1.01、2試験の異質性0%)、ラモトリギンは低めであった(効果量=0.70、3試験の異質性59%)
・躁症状:divalproexの1試験のみで効果量=0.91
(3)抗うつ薬
・2つ以上の試験で検討された抗うつ薬はなく、全て単一の小規模試験からの帰結で信頼性が乏しい。さらにrapid cyclingにおける抗うつ薬についてはSTEP-BDの帰結(病相回数の増加と関連)に要注意
・うつ症状に関して4試験合計の効果量は1.19であった(異質性52%)
(4)対照群(1つを除いてプラセボ群で構成)
・Global Impressionの対照群の効果量は全体で0.67(異質性0%)で、非定型抗精神病薬(全体の効果量、クエチアピン、オランザピン)、抗うつ薬(全体の効果量、シタロプラム)、気分安定薬(リチウム、バルプロ酸)の効果量の方が対照群よりも大きかった。気分安定薬全体の効果量は対照群と同等であった
・うつ症状:対照群の効果量(0.60、異質性51%)は、気分安定薬(全体、リチウム、ラモトリギン、バルプロ酸薬)、抗精神病薬(全体、クエチアピン、オランザピン)、抗うつ薬(全体、シタロプラム、エスシタロプラム、パロキセチン、ベンラファキシン)より数値的に低かった。甲状腺治療と同等の効果量であった(0.60)
・躁症状:対照群の効果量(0.33、異質性0%)は抗精神病薬(全体、クエチアピン、オランザピン/OFC、アリピプラゾール)と比較した場合、低い値であった。
・対照群の95%信頼区間との重なりがないことで有意な効果とみなした場合、うつ症状ではオランザピン(3試験)、シタロプラム(1試験)、ベンラファキシン(1試験)が対照群と比較して有意に有効性が高いと判断された。
・躁症状については、分析したすべての治療(非定型抗精神病薬)が対照群より有意に有効であった(クエチアピン、オランザピン、アリピプラゾール)。
議論
・一般的ではない解析を行ったため、結果の普遍性に疑問が生じる部分がある
・ベンラファキシンについては双極II型障害のみを対象とした試験からの帰結であるため一般化はできないだろう(特にSTEP-BDの帰結に反する点に注意が必要)
・クエチアピンについても急速交代型うつ病相において従来型のメタ解析でプラセボ群と有意差がみられるため、おそらく有効性が期待できる薬剤といえる(この論文の解析手法では入ってこない)
・うつ病相ではその他、オランザピンがよく、リチウムも効果量だけみると比較的良好
・Rapid cyclingの急性期躁症状に関しては気分安定薬による検討が極めて乏しい(1試験のみ)
・ルラシドンがどのように入ってくるのか、興味深いところ
文献1 Strawbridge et al. Acta Psychiatr Scand. 2022 Jul 2. doi: 10.1111/acps.13471. Online ahead of print -
SDM
2022年06月29日
・うつ病についてはMayo clinicなどでdecision aidが公表されており(https://depressiondecisionaid.mayoclinic.org/app/depression)、一部薬剤の性機能障害のリスクなどについてはCANMATガイドラインなどとも異なっており、?と思う部分もあるものですが、SDM(Shared Decision Making)の1つの形を提示したものとして興味深いものです。
・専攻医勉強会をする中で、初回エピソードの統合失調症において、このようなSDMができないものかと考えてみました。
・幸いなことに、ここ最近抗精神病薬の急性期治療(ただし初回エピソードについての試験は除く)における短期的な副作用発現リスクについてのメタ解析が出そろってきており、数字を並べるだけならある程度(貼付剤を除いて)可能な状況かと思います。
・ちなみに初回エピソード統合失調症における抗精神病薬の有効性については、APAガイドライン2020(https://psychiatryonline.org/doi/book/10.1176/appi.books.9780890424841)の記載「初回エピソードについて第2世代抗精神病薬では薬剤間の有効性の差は明らかではない。患者の特性と作用機序、副作用プロフィールに応じて選択する」や、BAPガイドライン2019( J Psychopharmacol. 2020 Jan;34(1):3-78. doi: 10.1177/0269881119889296. Epub 2019 Dec 12.)の記載「初発精神病の項目:薬剤選択については、特定の薬剤が別の薬剤と比較して有意に優れているとの明らかなエビデンスはない」にあるように、有効性の差について明白なエビデンスがない現状においては、忍容性を主体に薬剤選択をすることは合理的と思われます。
・実際には患者さん用になるべくわかりやすいスライドもつくってみたのですが、ここでは薬剤名を伏せ、ネットワークメタ解析の結果として提示された点推定値を主に用いて、薬剤毎のプロフィールをまとめてみます。
・データは主にM. Huhn et al. Lancet. 2019 Sep 14;394(10202):939-951. doi: 10.1016/S0140-6736(19)31135-3. Epub 2019 Jul 11)もしくはPillinger et al. Lancet Psychiatry. 2020 Jan;7(1):64-77.から引用しています。
薬剤A
・プロラクチン上昇:約7週間でプラセボとの平均差=-7.10ng/ml(男女混合の数値):有意差あり(有意に低下)
・眠気:対プラセボの相対リスク=1.46:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=1.30:有意差なし
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.32:有意差なし
・体重増加:平均7週間でプラセボ群との平均差=0.48kg:有意差なし
・血糖値上昇:6週間程度でプラセボとの平均差=2.34mg/dl:有意差なし
・コレステロール上昇:6週間程度でプラセボとの平均差=2.34 mg/dl:有意差なし
・中性脂肪上昇:6週間程度でプラセボとの平均差=1.76mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=1.95:有意差あり薬剤B
・プロラクチン上昇:約7週間でプラセボとの平均差=38ng/ml(男女混合の数値):有意差あり
・眠気:対プラセボの相対リスク=2.03:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=1.31:有意差あり
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.80:有意差あり
・体重増加:平均7週間でプラセボ群との平均差=1.44kg:有意差あり
・血糖値上昇:6週間程度でプラセボとの平均差=3.52mg/dl:有意差なし
・コレステロール上昇:6週間程度でプラセボとの平均差=2.34mg/dl:有意差なし
・中性脂肪上昇:6週間程度でプラセボとの平均差=3.52mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=2.73:有意差あり薬剤C
・プロラクチン上昇:約7週間でプラセボとの平均差=4.47ng/ml(男女混合の数値):有意差あり
・眠気:対プラセボの相対リスク=2.17:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=1.94:有意差あり
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.05:有意差なし
・体重増加:平均7週間でプラセボ群との平均差=1.94kg:有意差なし
・血糖値上昇:6週間程度でプラセボとの平均差=3.6mg/dl:有意差なし
・コレステロール上昇:6週間程度でプラセボとの平均差=15.6mg/dl:有意差あり
・中性脂肪上昇:6週間程度でプラセボとの平均差=40.5mg/dl:有意差あり
・アカシジア:7週間程度で対プラセボの相対リスク=0.99:有意差なし薬剤D
・プロラクチン上昇:約7週間でプラセボとの平均差=7.04ng/ml(男女混合の数値):有意差あり
・眠気:対プラセボの相対リスク=1.75:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=1.14:有意差なし
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.94:有意差あり
・体重増加:平均7週間でプラセボ群との平均差=0.32kg:有意差なし
・血糖値上昇:6週間程度でプラセボとの平均差=-5.22mg/dl:有意差あり(有意に低下)
・コレステロール上昇:6週間程度でプラセボとの平均差=-1.17 mg/dl:有意差なし
・中性脂肪上昇:6週間程度でプラセボとの平均差=0mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=3.93:有意差あり薬剤E
・プロラクチン上昇:約7週間でプラセボとの平均差=0.95ng/ml(男女混合の数値):有意差なし
・眠気:対プラセボの相対リスク=1.64:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=0.72:有意差なし
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.60:有意差なし
・体重増加:平均7週間でプラセボ群との平均差=0.70kg:有意差なし
・血糖値上昇:6週間程度でプラセボとの平均差=0.72mg/dl:有意差なし
・コレステロール上昇:6週間程度でプラセボとの平均差=1.95mg/dl:有意差なし
・中性脂肪上昇:6週間程度でプラセボとの平均差=-0.88mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=1.35:有意差なし薬剤F
・プロラクチン上昇:約7週間でプラセボとの平均差=48.51ng/ml(男女混合の数値):有意差あり
・眠気:対プラセボの相対リスク=1.33:有意差なし
・抗コリン系副作用出現リスク:対プラセボの相対リスク=1.42:有意差なし
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.61:有意差あり
・体重増加:平均7週間でプラセボ群との平均差=1.49kg:有意差あり
・血糖値上昇:6週間程度でプラセボとの平均差=3.52mg/dl:有意差なし
・コレステロール上昇:6週間程度でプラセボとの平均差=2.34mg/dl:有意差なし
・中性脂肪上昇:6週間程度でプラセボとの平均差=3.52mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=1.47:有意差なし薬剤G
・プロラクチン上昇:約7週間でプラセボとの平均差=-1.17ng/ml(男女混合の数値):有意差なし
・眠気:対プラセボの相対リスク=3.27:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=3.89:有意差あり
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=:有意差あり
・体重増加:平均7週間でプラセボ群との平均差=1.44kg:有意差あり
・血糖値上昇:6週間程度でプラセボとの平均差=1.62mg/dl:有意差なし
・コレステロール上昇:6週間程度でプラセボとの平均差=12.1mg/dl:有意差なし
・中性脂肪上昇:6週間程度でプラセボとの平均差=28.2mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=1.01:有意差なし薬剤H
・プロラクチン上昇:約7週間でプラセボとの平均差=5.05ng/ml(男女混合の数値):有意差あり
・眠気:対プラセボの相対リスク=2.17:有意差あり
・抗コリン系副作用出現リスク:対プラセボの相対リスク=1.11:有意差なし
・抗パーキンソン病薬併用リスク:対プラセボの相対リスク=1.21:有意差なし
・体重増加:平均7週間でプラセボ群との平均差=1.21kg:有意差あり
・血糖値上昇:6週間程度でプラセボとの平均差=-2.52mg/dl:有意差なし
・アカシジア:7週間程度で対プラセボの相対リスク=2.38:有意差あり・これらのほかにコスト、性機能障害(Serretti et al. Int Clin Psychopharmacol. 2011, 26;130-140)、遅発性ジスキネジア(Carbon M. et al World Psychiatry 2018 Oct;17(3):330-340. doi: 10.1002/wps.20579.)などのリスクについても言及していいと思いますが、ここでは省略します。
・このままではSDMに使用できないと思われるので、例えば
「抗精神病薬の副作用には様々なものがあります。以下の副作用の中からあなたが避けたい副作用を、重視するものから順に順位付けをしてください
( ) 手のふるえや筋肉のこわばりなどのパーキンソン症状
( ) 体重増加
( ) プロラクチンというホルモンの増加による無月経など
( ) 性機能障害
( ) 眠気
( ) 口の渇きや便秘など
( ) 足がむずむずするアカシジアという副作用
( ) 血糖値やコレステロール、中性脂肪の増加」
などの質問をしてみるのは良い方法かもしれません。・これについては、中込先生の論文(中込和幸 臨床精神薬理 14:688-703,2011)を参照すると、患者さんへの困っている副作用についてのアンケート結果から、口渇、体重増加、眠気、月経不順(高プロラクチン血症)が上位であることがわかります。
・この順番で上記薬剤を選択すると、最終的に薬剤A、E、ついで薬剤Dが残りそうなことがわかります。LAI製剤があることや、クロザピン治療につなげうる薬剤であることを考慮すると(CP換算600mgまで投与できる)、薬剤Aが最有力候補となります。これは日本臨床精神神経薬理学会のアルゴリズム委員会が作成した初回エピソード統合失調症に対する治療アルゴリズム(Takeuchi H. et al. Hum Psychopharmacol. 2021 Nov;36(6):e2804. doi: 10.1002/hup.2804. Epub 2021 Jul 9.)の第1選択薬と同じであり、アルゴリズムが妥当性を支持する結果と思われます。ただし、SDMで患者さんが別の薬剤を選択する可能性もあるため、その場合には異なる薬剤で治療を開始することもありうるでしょう
-
KCNQ2
2022年06月21日
・KCNQ2チャネルといえば2月のScience誌の論文(Li SB et al. Science. 2022 Feb 25;375(6583):eabh3021. doi: 10.1126/science.abh3021. Epub 2022 Feb 25.)で、加齢に伴う発現低下がオレキシン神経の興奮閾値の低下と発火頻度の上昇をもたらし、睡眠の断片化につながるのではないかということがマウスの実験により報告されたことが記憶に新しいところです。
・今回はケタミンの作用機序にこのチャネルに関与しているのではないかという報告(文献1)です。
ケタミンとKCNQ2チャネル
背景
・ケタミンの抗うつ作用がケタミン代謝後も持続することから、その作用機序は、NMDA受容体阻害作用やAMPA受容体の機能活性化のみに起因するとは考えにくい。下流のシグナル伝達カスケードが活性化され、うつ病に関与する主要な脳領域や神経回路に長期的かつ持続的な適応がもたらされることが考えられる。ケタミンの作用機序はまだよくわかっていない。特にケタミンが細胞特異的にどのような遺伝子発現の変化などをもたらすのかは明らかではない
・今回、マウスにおいて、single cell RNA-seq(scRNA-seq)を用いてケタミンを単回投与した際の、単一細胞レベルでの遺伝子発現の変化を観察し、海馬腹側における数千個の細胞について、ケタミンないし生食投与前後でのトランスクリプトームの変化を解析した。
]・その結果、グルタミン酸作動性神経における、KCNQ2チャネルの発現変化がケタミン作用の重要な下流制御因子として同定された
以下の3点が主な結果となる
(1)KCNQチャネルを薬理学的に操作するとケタミンによるマウスへの抗うつ作用が変化するため、ケタミンの抗うつ作用はKCNQチャネルを介したものであると考えられること、
(2)KCNQ活性化剤であるretigabineのケタミンとの同時投与がケタミンの効果を増強すること
(3)KCNQチャネルへの薬理学的作用は従来の抗うつ薬(エスシタロプラム)では模倣できないため、KCNQチャネルの抗うつ作用への関与はケタミンに特異的であると考えられること方法と結果
・マウスの海馬腹側より採取された数千の細胞は遺伝子発現プロフィールに応じて分類された。Uniform manifold approximation and projection (UMAP) plotsを用いて可視化したところ、細胞群が13のクラスター(グルタミン酸作動性神経細胞、GABA作動性神経細胞、オリゴデンドロサイト、オリゴデンドロサイト前駆細胞、アストロサイト、内皮細胞、ミクログリア、マクロファージ、上衣細胞、周皮細胞、髄膜細胞、血管細胞、血液細胞)に分類された。
・ケタミン投与による遺伝子発現の変化において、生食投与時の変化と比較して、有意な発現量の差異がみられたのは、合計263種類の遺伝子であった。うち135種類はグルタミン酸作動性神経細胞でのみ、アストロサイトのみが27種類、オリゴデンドロサイトのみが16種類、オリゴデンドロサイト前駆細胞のみが3種類、内皮細胞のみが1種類、血管細胞のみが1種類の遺伝子発現に有意な差異がみられた。
・続いて、遺伝子発現の変化の差異の大きかった3種類の細胞について、細胞内のどのようなシグナル伝達経路が変化しているのかを調べるためにパスウェイ解析(pathway enrichment analysis)を行った。
・その結果、グルタミン酸作動性神経細胞では、ケタミン投与により、カルシウムシグナル伝達経路、シナプス機能と可塑性、神経変性疾患などに関わる多くのシグナル伝達経路の変化が明らかになった。アストロサイトでは、脂肪酸伸長、ギャップジャンクション、ファゴソーム活性、アルツハイマー病で異常がみられる経路などが有意な経路として抽出。一方、オリゴデンドロサイトでは、ビタミン消化、吸収、脂肪酸伸長などに関わる伝達経路の有意な変化が抽出された。
・続いて、グルタミン酸作動性神経細胞がtdTomatoにより蛍光標識されているモデルマウスを作成した。さらに海馬腹側より採取した細胞を蛍光活性化セルソーティング(fluorescence-activated cell sorting)によりtdTomato陽性細胞(グルタミン酸作動性神経細胞)とそれ以外のtdTomato陰性細胞に分類した。
・グルタミン酸作動性神経細胞でケタミン投与による発現量の変化が大きかった8種類の遺伝子について、定量的リアルタイムポリメラーゼ連鎖反応によりその変化量を定量化したところ、kcnq2遺伝子が最も発現変化量の大きな遺伝子として同定された。
・続いて電気生理学的実験により実際にKCNQチャネルの発現増加が起きているかどうかを検証した。
・kcnq2遺伝子は、神経細胞の興奮性の制御に重要な役割を果たす緩徐電位依存性カリウムチャネルであるKv7.2タンパク質をコードしている
Kv7.2およびKv7.3タンパク質(Kcnq3遺伝子)は、KCNQ(Kv7)ホモないしヘテロ4量体を形成し、M電流を発生させ、神経細胞の全体の興奮性を調節している。・whole-cell voltage-clamp recordingsによりケタミン投与前後でのM電流密度を測定したところ、ケタミン投与後には生食投与後と比較して、有意なM電流密度の増加が観察され、ケタミン投与がKCNQチャネルの有意な増加をもたらすことを示唆する所見が得られた
・kcnq2遺伝子の発現は増加していたが、kcnq3遺伝子の発現の増加はみられなかった
・kcnq2が神経細胞で特異的に発現しているのに対し、Kncq3は神経細胞、アストロサイト、オリゴデンドロサイト、およびオリゴデンドロサイト前駆細胞などで発現している。これらの知見は、Kcnq2が海馬の神経細胞において重要かつより集中的な役割を果たしていることを示唆するものである
・このことを検証するため、アデノ随伴ウイルスベクターを用いて海馬腹側のkcnq2遺伝子発現をノックダウンした場合に、ケタミン投与後の強制水泳試験の成績が変化するかどうかを検討した。
・対照群ではケタミン投与後に強制水泳試験での無動時間が有意に減少したが、ノックダウン群では、生食投与群とケタミン投与群とで有意差はみられなかった。このことは海馬におけるkcnq2遺伝子発現がケタミンの抗うつ作用発現にとって重要であることを示唆するものである
・続いて慢性ストレスが、kcnq2遺伝子発現に与える影響を調べるため、モデルマウスに10日間の慢性社会的敗北ストレスを負荷し、海馬における発現量の変化を検討した
・その結果海馬腹側のグルタミン酸作動性神経細胞におけるKcnq2 mRNA発現量の有意な減少が観察された
・慢性ストレス曝露後のマウスにケタミンを投与した場合に、海馬のグルタミン酸作動性神経細胞におけるkcnq2 mRNAの発現量がどのようになるかを評価したところ、慢性ストレス曝露後のケタミン投与はkcnq2発現量をベースラインレベルまで回復させた
・続いてケタミン投与によるkcnq2発現増加の細胞内機序を調べるため、kcnq2遺伝子発現に影響を与えうるシグナル経路(カルシウムイオン、カルモジュリン、カルシニューリン、Aキナーゼアンカリングタンパク質5)について、ケタミンがどの経路を介してkcnq2遺伝子発現の亢進をもたらすのかを調べた
・各シグナル経路の薬理学的阻害による影響を検討した。ケタミン活性代謝物(HNK)投与ないし生食投与と、ニフェジピン(L型カルシウムチャネル阻害剤)、W-7 hydrochloride(カルモジュリン阻害剤)、シクロスポリン-A(カルシニューリン阻害剤)のいずれかの組み合わせで評価したところ、いずれの投与もケタミンによるkcnq2発現亢進を阻害した。
・ケタミン投与によるL型カルシウムチャネル経路、カルモジュリン経路およびカルシニューリン経路の活性化がkcnq2発現亢進において重要な役割を果たすことを示唆する
・kcnq2阻害剤(XE991)を投与すると、ケタミンを投与しても強制水泳試験における無動時間の有意な減少はみられなくなった。ケタミンが抗うつ作用を発揮するためには、KCNQチャネル活性化が必要であることを示唆するものである
・一方で、KCNQチャネルアゴニストであるretigabineを投与すると、単独では抗うつ作用はみられなかったが、ケタミンと併用すると、ケタミン単独投与時よりもさらに有意に強制水泳試験の結果が良好なものとなった。Retigabineがケタミンの作用を増強する可能性を示唆するものである。ただしretigabineの用量が高用量となると、この効果は消失した。これは、ケタミンの逆U字型の用量効果曲線と一致するものである
・最後にretibabineによる抗うつ作用増強効果がケタミン併用時のみなのか、それとも他の抗うつ薬と併用してもみられるのかを検討した
エスシタロプラムにretigabineを併用しても強制水泳試験での無動時間のさらなる減少、効果の増強はみられなかった。Retigabineによる増強効果はケタミンと併用時のみみられるものであった・エスシタロプラム投与による海馬におけるkcnq2遺伝子発現の有意な増加は観察されなかった
議論
・今回、初めてscRNA-seqを用いてケタミン投与による細胞特異的な分子機構を明らかにした
・今回の結果は、ケタミンによる抗うつ作用のメカニズムの一部を説明しうる可能性がある
・ケタミン投与の際にニフェジピンなどCaブロッカーを内服している患者はケタミンの効果が乏しいのか?臨床的のそのようなデータはあるか?
・今回の結果によると、ケタミン処理により、in vivoでは処理後2日、in vitroでは最大6時間後にグルタミン酸作動性神経細胞におけるKcnq2 mRNAの発現が増加する。ケタミンは海馬腹側のグルタミン酸作動性神経細胞においてカルモジュリン/カルシニューリン/AKAP5/NFAT転写経路を介してkcnq2発現亢進をもたらし、その持続的抗うつ作用を誘導している可能性がある。
・ケタミン治療の際にretigabineを併用するとさらにその効果が増強するかもしれない
コメント
2021年にはうつ病に対してretigabineの小規模RCTの結果が報告され期待のもてる結果になっています(Am J Psychiatry. 2021 May 01; 178(5): 437–446. doi:10.1176/appi.ajp.2020.20050653)。小規模試験なのでこの試験だけで有効性に関する結論は出せませんが、今後ケタミンとの併用やさらに大規模な介入試験での検証が望まれるとこです。
文献1:Juan Pable Lopez et al. Neuron. 2022 May 25;S0896-6273(22)00409-3. doi: 10.1016/j.neuron.2022.05.001. Online ahead of print
-
ここ最近の勉強会のこと
2022年06月12日
・ここ最近の振り返りという事でまとめておきます。院内勉強会で扱ったものについてはまた後日まとめたいと思います。専攻医勉強会では統合失調症の急性期治療に関連した内容に入り、いくつかの論文をまとめたスライドで話を進めています。急性期治療に関するスライドに含めた論文は、以下のようなものになります。
1.Huber et al. Schizophrenia Bulletin, Volume 6, Issue 4, 1980, Pages 592–605
・まだ統合失調症の診断にSchneiderとBleulerの基準も用いられていた1950年代からの調査も含めて長期臨床経過を分類した論文。最近でも引用されることがあるようです。2.井上 新平ら「統合失調症の臨床疫学」:臨床精神医学 34(7):855-861.2005
・いわずとしれたDOSMed試験などの長期経過のまとめられた論文3.Maren Carbon, Christoph U. Correll Dialogues Clin Neurosci. 2014 Dec; 16(4): 505–524
・これも専門医試験に出題されうる経過の図(各病相間の移行割合など)が入っているのでとりあげました。4.BAPガイドライン J Psychopharmacol. 2020 Jan;34(1):3-78. doi: 10.1177/0269881119889296. Epub 2019 Dec 12.
・CHR、初発精神病などにわけて詳しくエビデンスが解説してあるのがいいです5.M. Huhn et al. Lancet. 2019 Sep 14;394(10202):939-951. doi: 10.1016/S0140-6736(19)31135-3. Epub 2019 Jul 11
・有効性に関する解析については、文献25の論文にもあるように、プラセボ反応率が年代によって変化しているので、appendixのプラセボ反応率で調整したネットワークメタ回帰分析の図の方がよりバイアスが少ないと思われること。一方で副作用については客観性が高い指標も多いため、副作用については有用と思われることから多く引用しました。6.Harringan et al. J Clin Psychopharmacol. 2004 Feb;24(1):62-9. doi: 10.1097/01.jcp.0000104913.75206.62.
・QT延長について調べた論文。ベースラインにQT延長がなく、通常使用する用量の範囲内では、その薬剤の代謝に関わるCYP阻害作用のある薬剤と併用していてもそこまで心配しなくてもよさそうというもの7.EUFEST study : Lancet. 2008 Mar 29;371(9618):1085-97
・オープンラベル試験ですが、各薬剤の継続率に差があることと、継続できさえすれば有効性指標についての経時変化はほぼ変わらないことなどが示されています。8.PAFIP study:Int J Neuropsychopharmacol. 2020 Apr 23;23(4):217-229. doi: 10.1093/ijnp/pyaa004.
・これもオープンラベルですが継続率の違いや、初回エピソードにおける性機能障害の副作用について詳細な図があるのが注目点となります9.McEvoy et al. Am J Psychiatry. 2007 Jul;164(7):1050-60. doi: 10.1176/ajp.2007.164.7.1050.
・早期精神病における二重盲検試験10.Emsley R, Rabinowitz J, Medori R; Early Psychosis Global Working Group. Schizophr Res. 2007 Jan;89(1-3):129-39. Epub 2006 Nov 7.
・初発精神病における二重盲検試験11.Green AI et al; HGDH Study Group. Schizophr Res. 2006 Sep;86(1-3):234-43. Epub 2006 Aug 2.
・初発精神病における二重盲検試験。オランザピンの体重増加が強烈です。その他の薬剤もですが初回エピソードでは副作用が出やすいことを示唆するものです。12.Moller et al. Int J Neuropsychopharmacol. 2008 Nov;11(7):985-97. doi: 10.1017/S1461145708008791. Epub 2008 May 9
・初回エピソード統合失調症における二重盲検試験。ハロペリドールのEPSの出現のしやすさなど。13.Cheng et al. J Psychopharmacol. 2019 Oct;33(10):1227-1236. doi: 10.1177/0269881119872193. Epub 2019 Sep 5.
・初回エピソード統合失調症における二重盲検試験。リスペリドンと比較したアリピプラゾールの特性がいろいろな指標の経時変化で示されています14.Kim et al. NPJ Schizophr. 2021 May 25;7(1):29. doi: 10.1038/s41537-021-00158-z.
・早期統合失調症におけるアリピプラゾールとD2アンタゴニストの比較のメタ解析など15.Zhu et al. Lancet Psychiatry. 2017 Sep;4(9):694-705
・初回エピソード統合失調症のネットワークメタ解析。初回エピソードに対する試験そのものが少ないため、比較対象となる薬剤の種類やデータが乏しく、確定的な結果が出せない現状がわかります。16.Hiroyoshi Takeuchi et al. Neuropsychopharmacology (2019) 44:1036–1042; https://doi.org/10.1038/s41386-018-0278-3
・初回エピソードと2回目のエピソードで同じ薬剤を使用しても有効性が異なることを報告したもの。貴重な報告です。17.APA guideline 2020:https://psychiatryonline.org/doi/book/10.1176/appi.books.9780890424841
・BAPガイドラインに比べてざっくりとした記載の印象ですが、各薬剤の副作用比較の図とかはわかりやすいです。ネット公表版では図の一部が欠落してて不完全です。18.Hitoshi Sakurai et al. Pharmacopsychiatry. 2021 Jan 12. doi: 10.1055/a-1324-3517
・日本臨床精神神経薬理学会のエキスパートコンセンサスです19.Hiroyoshi Takeuchi et al. Hum Psychopharmacol. 2021 Nov;36(6):e2804. doi: 10.1002/hup.2804. Epub 2021 Jul 9.
・日本臨床精神神経薬理学会の治療アルゴリズムです20.Lee et al. Clin Psychopharmacol Neurosci. 2020 Aug 31;18(3):386-394. doi: 10.9758/cpn.2020.18.3.386.
・韓国でのアルゴリズムです21.日本神経精神薬理学会 統合失調症薬物治療ガイドライン 2015(2017年改訂)
22.日本神経精神薬理学会 統合失調症薬物治療ガイドライン 2022
・2017年改訂版でのCQ1-4が無くなってしまったことと、そのかわりになる論文が文献23で示されています。23.Hui et al. Int J Neuropsychopharmacol. 2022 Apr 22:pyac002. doi: 10.1093/ijnp/pyac002. Online ahead of print.
・Asian Network of Early Psychosis Wriing Groupによる素晴らしいガイドライン。10年予後で有名なDr.Huiらのグループが精力的に初回エピソードと治療中断可能性の問題に取り組んでこられてきたことがよくわかるものです。24.CU Correll et al. NPJ Schizophr. 2022 Feb 24;8(1):5. doi: 10.1038/s41537-021-00192-x.
・各ガイドラインの比較の系統的レビュー25.S. Leucht et al. Am J Psychiatry. 2017 Oct 1;174(10):927-942. doi: 10.1176/appi.ajp.2017.16121358. Epub 2017 May 25.
・プラセボ反応率が年々違うことや、プラセボ反応率に影響しうる要因などを解析したもの。結果はなかなか興味深いです。26.Schneider-Thoma et al. Lancet. 2022 Feb 26;399(10327):824-836. doi: 10.1016/S0140-6736(21)01997-8
・維持療法期のネットワークメタ解析。主要評価項目の解析にBayesian NMAを使用しており、そのため文献27と結果が一部異なります。27.Giovanni Ostuzzi et al. World Psychiatry. 2022 Jun;21(2):295-307. doi: 10.1002/wps.20972
・維持療法期のネットワークメタ解析。文献26と比べてサンプルサイズが50未満の試験は除外するなどinclusion criteriaの違いはありますが、主要評価項目の解析にFrequentist NMAを用いており、文献26との結果の違いの原因となっています。28.JE Thomas et al. Curr Neuropharmacol. 2015;13(5):681-91. doi: 10.2174/1570159x13666150115220221.
・ルラシドンやアセナピンなどのアカシジア出現頻度を以前からの第2世代薬と比較したものです。抗コリン作用が乏しい分、出現しやすいのかと思います。29.Carbon M. et al. World Psychiatry 2018 Oct;17(3):330-340. doi: 10.1002/wps.20579.
・アリピプラゾールの遅発性ジスキネジア出現リスクが頭一つ抜けて有意に少ないことをmoderation analysisで示したものです。30.H Taipale et al. Lancet Psychiatry. 2021 Aug 30;S2215-0366(21)00241-8. doi: 10.1016/S2215-0366(21)00241-8
・プロラクチンと乳癌リスクに関してのnested case-control研究。長期投与に際して重要な結果かと思います31.Pillinger et al. Lancet Psychiatry. 2020 Jan;7(1):64-77.
・抗精神病薬の代謝系副作用についてのネットワークメタ解析です。中性脂肪などのデータは他にないものになります。32.H. Wu et al. Wu et al. Schizophr Bull. 2022 May 7;48(3):643-654. doi: 10.1093/schbul/sbac001
・抗精神病薬と体重増加に関するdose-response meta-analysisです。dose-response meta-analysisは恣意的な操作が入っている解析ではありますが、図がきれいでいいですね。33.J Greger et al. J Clin Psychopharmacol 2021;41: 5–12
・後方視的なチャートレビューのため質は高くはないのですが、長期的な代謝系副作用についての報告です34.S. Leucht et al. Am J Psychiatry. 2020 Apr 1;177(4):342-353. doi: 10.1176/appi.ajp.2019.19010034. Epub 2019 Dec 16.
・各抗精神病薬の短期的有効性に関するdose-response meta-analysisです35.S. Leucht et al. JAMA Psychiatry. 2021 Nov 1;78(11):1238-1248.
・維持療法期におけるdose-response meta-analysis36.H. Taipale et al. Lancet Psychiatry. 2022 Apr;9(4):271-279. doi: 10.1016/S2215-0366(22)00015-3. Epub 2022 Feb 16
・大規模コホートによる抗精神病薬の用量と再燃リスクについての報告で、0.9~1.1DDD投与した場合と比較して0.6DDD未満だと明らかに再燃リスクが増大することを示し、かつ再燃を繰り返すたびに抗精神病薬の用量が増えていくことをWithin-individual modelで示した観察研究です。37.J. Tiihonen et al. JAMA Psychiatry. 2019 May 1;76(5):499-507.
・大規模コホートによる単剤療法と併用療法の再入院リスクをwithin-individual analysisで比較した報告です。観察研究なのでバイアスリスクはありますが、このような解析は大規模コホートならではとなります。38.I. Bighelli et al. Lancet Psychiatry. 2021 Nov;8(11):969-980. doi: 10.1016/S2215-0366(21)00243-1. Epub 2021 Oct 12.
・再燃予防における心理的介入のネットワークメタ解析です。通常治療のみと比較して、家族関係介入などが大幅に再燃リスクを減らしている結果は重要なものです。39.Cochrane Database Syst Rev. 2018 Nov 15;11(11):CD008712
・CBT対その他の心理的介入の再発・再燃リスクの比較40.三宅 誕実ら 臨床精神薬理 15:1099-1107,2012
・統合失調症におけるうつ症状の総説です41.S. Leucht et al. Lancet. 2009 Jan 3;373(9657):31-41. doi: 10.1016/S0140-6736(08)61764-X. Epub 2008 Dec 6.
・2009年の古いメタ解析ですが、第1世代と第2世代の比較を引用しました42.B Galling et al. Acta Psychiatr Scand. 2018 Mar;137(3):187-205. doi: 10.1111/acps.12854.
・統合失調症における抗うつ薬増強のエビデンスです。有効性は乏しいものですが、統合失調症における抗うつ薬の使用は少なくとも全体として陽性症状などを有意に悪化させることはなさそうです。43.M. Krakowski et al. Am J Psychiatry. 2021 Mar 1;178(3):266-274. doi: 10.1176/appi.ajp.2020.20010052. Epub 2021 Jan 21.
・統合失調症と攻撃性に関する比較試験です44.L Citrome et al. Psychiatr Serv. 2001 Nov;52(11):1510-4. doi: 10.1176/appi.ps.52.11.1510.
・これも統合失調症と敵意、攻撃性に関する試験です。45.A. Serretti et al. Int Clin Psychopharmacol. 2011 May;26(3):130-40. doi: 10.1097/YIC.0b013e328341e434.
・性機能障害についてのメタ解析です。46.Yaara Zisman-Ilani et al., JAMA Psychiatry. 2021 Nov 1;78(11):1183-1184
・SDMについて47.中込和幸 臨床精神薬理 14:688-703,2011
・アドヒアランスについての総説です・今年に入って2月と6月に維持療法期間における抗精神病薬の有効性に関するネットワークメタ解析の報告が2報(26と27)でて、細かいところで結果がかなり異なる部分があり、inclusion criteriaの違いかと思って、frequentist NMAでいろいろやってみたのですが違いを再現できず、Prof. Stefan Leuchtにメールで聞いてみたら筆頭著者のDr. Schneider-Thomaにつないでいただき教えていただきました。一言でいえばFrequentist NMAとBayesian NMAの違いということらしいです。昨年に引き続き親切に教えていただいてありがとうございます。




